作 者:张静宜(住院医师 郑州人民医院消化内科)
指导者:马英杰(主任医师 郑州人民医院消化内科)
AIP被认为是一种IgG4相关性系统性疾病,最早是由Yoshida等在1995年提出的,之后AIP及与其发病机制相类似的疾病逐渐被确立为一种独特的疾病谱。IgG4相关性消化疾病多数以AIP为基础病变,同时可伴有胆管、胆囊、肝门区等受累,其相关疾病包括AIP、IgG4相关性硬化性胆管炎(IgG4-sclerosing cholangitis,IgG4-SC)、IgG4相关性涎腺炎(IgG4-associated sialadenitis,IgG4-AS)、IgG4相关性自身免疫性肝炎(IgG4 associated autoimmune hepatitis,IgG4-AIH)。由于IgG4阳性浆细胞和淋巴细胞大量浸润伴随着纤维化,可同时或不同时发生弥漫性或局灶性器官肿大、包块形成或小结节性损害。AIP最常见或首发的症状多为阻塞性黄疸,多表现为波动性黄疸,同时可伴有腹痛或背部放射性痛、体重减轻或厌食等。糖尿病是较常见的并发症,尤其好发于Ⅱ型AIP,多伴有轻度至中度外分泌功能损伤。胰腺外表现有涎腺或泪腺肿大,因腹膜后纤维化或间质性肾炎、肾积水致腰痛,因肺部病灶致呼吸道症状等。
影像学表现:①CT:胰腺弥漫性肿大以及胰管轮廓消失是AIP的典型影像学表现。在T1加权成像上,受累的胰腺与肝脏相比,信号降低,同时由于纤维炎性病变累及胰周脂肪组织,其在CT上呈低密度影,而在T2加权成像上呈低信号影,包裹胰腺。②超声:低回声胰腺实质内可见散在高回声区域;主胰管不规则的狭窄(管腔直径<3mm)也是AlP的特征;节段性病变,通常表现为肿块型病灶,与胰腺癌的鉴别困难。
病理表现:Ⅰ型AIP即IgG4相关性AIP,又称LPSP:①大量浆细胞和淋巴细胞浸润,其中浆细胞每高倍视野可见大于10个IgG4阳性细胞,且IgG4/IgG大于40%;②独特的席纹状或漩涡状纤维化;③静脉周围的淋巴细胞和浆细胞浸润导致的闭塞性静脉炎。Ⅱ型AIP属非IgG4相关性胰腺炎,临床特征为胰腺体积增大,组织学无或极少IgG4阳性浆细胞。血清IgG4>1350mg/L作为诊断的最佳截断值,其敏感性和特异性分别为97.0%和79.6%。
1.患者基本情况
患者:男性,66岁。
主诉:食欲不振、乏力、困倦伴消瘦1个月。
现病史:1个月前,患者无明显原因出现食欲不振,进食量较前下降约1/2,伴乏力、困倦,体重下降约5kg,无腹痛、腹胀、恶心、呕吐或黑便,无反酸、胃灼热、腹泻、发热,无心悸、胸闷,未服药。发病以来,患者神志清、精神尚可,饮食差,睡眠一般,大小便未见异常。
既往史:患高血压病8年,服用非洛地平缓释片;患糖尿病5年,服用二甲双胍;22年前患急性黄疸型肝炎,治愈;否认结核传染病史。
个人史:吸烟20年余,每日约20支。
家族史:无特殊。
2.入院查体
神志清,精神尚可,营养中等,巩膜无黄染,睑结膜无苍白,浅表淋巴结未触及肿大,心肺未闻及明显异常。腹软,无压痛及反跳痛,腹部未触及包块,肝脏、脾脏肋下未触及,Murphy征阴性,移动性浊音阴性,肝区、双肾区无叩击痛,肠鸣音4次/min。双下肢无水肿。
3.入院辅助检查
血常规:白细胞计数6.36×109/L,红细胞计数4.31×1012/L,血红蛋白133g/L,中性粒细胞计数3.94×109/L,单核细胞计数0.22×109/L,嗜碱性粒细胞计数0.02×109/L,嗜酸性粒细胞计数0.46×109/L,淋巴细胞1.72×109/L,血小板计数229×109/L。血糖21.00mmol/L,糖化血红蛋白10.90%,尿糖3+。C反应蛋白11.4mg/L(正常参考值:0.068~8.2mg/L),红细胞沉降率51mm/第1h末(正常参考值:0~15mm/第1h末),降钙素原0.025ng/mL(正常参考值:0~0.05ng/mL),淀粉酶 181U/L(正常参考值:15~115U/L),脂肪酶307U/L(正常参考值:0~60U/L)。肝功能:丙氨酸氨基转移酶13IU/L,天冬氨酸氨基转移酶11IU/L,碱性磷酸酶105IU/L,谷氨酰转肽酶18IU/L,总胆红素15.1µmol/L,间接胆红素11.8µmol/L,总蛋白81.3g/L,白蛋白45.5g/L,白球比1.27。肾功能:尿素7.30mmol/L,肌酐117µmol/L,尿酸 361µmol/L。血脂:总胆固醇4.00mmol/L,甘油三酯 2.50mmol/L,高密度脂蛋白胆固醇0.90mmol/L,低密度脂蛋白胆固醇2.47mmol/L,载脂蛋白A-1 0.81g/L(免疫浊度法),载脂蛋白B 0.97g/L(免疫浊度法)。结明三项(结明试验、ICT-TB卡试验、快速TB卡试验):TB-DOT 阳性(+),TB-ChecK(1)(-),TB-Ig(-)。皮质醇:早 8 点 12.93µg/dL(正常参考值:8.7~22µg/dL),下午 4 时 4.75µg/dL(正常参考值:8.7~22µg/dL)。甲状腺功能:游离甲状腺素15.76pmol/L(正常参考值:7.9~14.4pmol/L),游离三碘甲状腺原氨酸4.62pmol/L,促甲状腺激素 1.35mIU/L。肿瘤标记物:CEA、CA199、CA724、CA125、CA153、AFP、CA50、NSE正常,CY211 5.75ng/mL(正常参考值:0.1~2.38ng/mL)。肝胆脾胰彩超:胰腺体尾部体积增大、回声减低(范围约71mm×31mm),主胰管未见扩张,胆囊壁毛糙。
4.初步诊断思维过程
(1)入院时病情总结
该患者为中老年男性,病史1个月,以食欲不振、消瘦为主要表现,超声检查提示胰腺体尾部增大、回声减低,淀粉酶、C反应蛋白升高,血沉增快。
(2)入院时诊断思路
患者为中老年男性,出现食欲不振及消瘦1个月,超声检查提示胰腺体尾部增大、回声减低,很容易与胰腺癌的黄疸、腹痛、体重下降三大症状关联,但相关肿瘤指标CA199不高,不支持该诊断,需行增强CT、MR、EUS等鉴别。另一个可能的诊断是慢性胰腺炎。慢性胰腺炎临床主要表现为腹痛、消化不良、胰源性糖尿病、体重减轻等;超声检查见胰腺体积增大或萎缩、边缘不整,胰腺实质回声变化、团块、钙化,胰管扩张等。有15%的慢性胰腺炎患者可无腹痛或腹痛轻。故该病例亦不能排除慢性胰腺炎诊断。CT、MR、ERCP有助于诊断慢性胰腺炎。该患者TB-DOT阳性,故虽罕见,也不能完全排除胰腺结核的可能,胰腺组织穿刺病理有助于明确诊断。综上分析,下一步应行CT、MR、MRCP、胰腺组织穿刺病理进行鉴别。
(3)入院初步诊断
①食欲不振待查,胰腺癌或慢性胰腺炎可能;②高血压病;③2型糖尿病。
5.后续检查
腹部CT:胰体尾部形态饱满,边缘毛糙,周围可见渗出影,密度不均匀,边缘欠清。左侧肾筋膜囊增厚。
增强CT:胰腺体尾部体积增大,形态饱满,边缘平直,似呈腊肠样改变,周围可见少量渗出影,与左侧肾筋膜粘连,左侧肾筋膜囊增厚。增强扫描显示动脉期胰腺体尾部均匀强化,程度低于胰腺头颈部,静脉期持续渐进性强化,呈等密度改变,包绕脾静脉致脾静脉明显变窄,延时期体尾部强化程度高于头颈部,胰腺周围见多发直径小于7mm均匀强化结节。诊断意见:胰腺体尾部病变,伴周围渗出、淋巴结增大及脾静脉浸润,考虑肿瘤性病变可能,不除外自身免疫型胰腺炎。
磁共振平扫+增强:增强扫描显示胰体尾部、胰头部病变强化程度及节律近似,动脉期呈轻度不均匀强化,静脉期持续强化,信号强度与正常胰腺实质相近或略高,延迟期呈相对较高信号。胰管未见扩张。脾动脉、脾静脉局部被包绕,前者管壁僵硬,管腔局部轻度狭窄,后者局部显示中断。诊断意见:胰头部结节影,胰体尾部肿大,伴脾动静脉受累,多考虑自身免疫性胰腺炎可能(图1)。
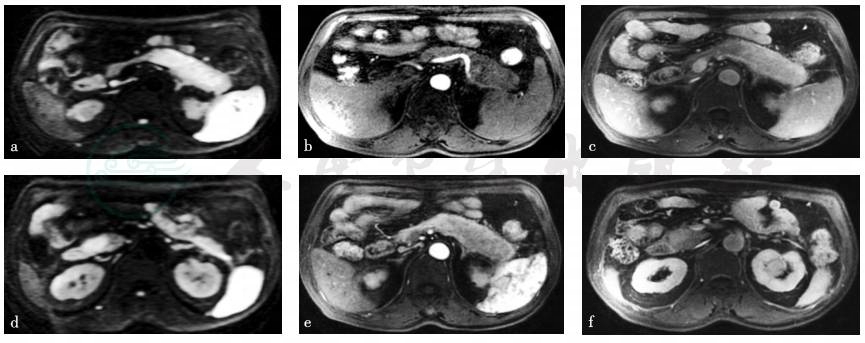
图1 磁共振成像[弥散加权成像技术(diffusion weighted imaging,DWI)、增强早期+晚期、门脉期]
引自:消化系统疑难疾病诊疗思维及病例解析.第1版.ISBN:978-7-117-28669-5.主编:
进一步完善检查:免疫球蛋白:IgM 0.46g/L(正常参考值:0.6~5.0g/L),IgA 2.51g/L,IgG 16.50g/L,IgG4 8.73g/L(正常参考值:0~2.01g/L);CA50 25.47U/mL(正常参考值:0~25U/mL);抗核抗体(核颗粒+核均质1∶100);抗髓过氧化物酶抗体IgG阴性;抗蛋白酶3抗体IgG阴性;抗线粒体抗体阴性;抗肝细胞溶质抗原1型抗体阴性;抗平滑肌抗体阴性;抗肝-肾微粒体抗体(1)阴性;nRNP/Sm阴性;Jo-(1)阴性;核小体阴性;SS-A阴性;SS-B阴性;SCL-(70)阴性;sm阴性;抗双链DNA(免疫印迹)阴性;抗着丝点抗体阴性;组蛋白阴性;核糖体P蛋白阴性;Ro-52阴性;心磷脂抗体阴性;抗蛋白酶3抗体IgG阴性;抗髓过氧化物酶抗体IgG阴性;抗RA33抗体15.90U/mL(正常参考值:0~20U/mL);抗环瓜氨酸肽0.5U/mL(正常参考值:0~5U/mL)。CT引导下胰腺穿刺病理:送检胰腺组织正常腺泡结构消失,残存导管上皮未见异型,间质弥漫炎细胞浸润伴纤维化,浸润炎细胞以浆细胞为主,符合IG4相关的自身免疫性疾病。免疫组化:CK上皮+,CgA胰岛+、Syn胰岛+、CD56胰岛+、Ki67 少量炎细胞 +、CD38 浆细胞+、CD138浆细胞 +、IgG4(+)、IgG(+),IgG4/IgG>40%,IgG4>10个。磁共振全身类PET成像未见胰腺外组织脏器累及。
6.最终诊疗思维过程
影像学表现在自身免疫性胰腺炎(autoimmune pancreatitis,AIP)的诊断中占有至关重要的位置。该病的影像学特点为胰腺呈弥漫性、局限性或局灶性肿大,典型者为“腊肠样”改变,部分不典型病理可出现局部肿块;主胰管弥漫性变细或局限性狭窄,病变累及胆总管下段时可造成局部呈陡然向心性狭窄;由于胰周积液、炎症或脂肪组织纤维化而出现胰周“鞘膜”征,增强时表现为动脉期密度略低,延迟期均匀强化。事实上,部分AIP的诊断与放射科医师的典型描述和有价值的提示密不可分。诊断AIP的标准还应包括IgG4水平及组织学证据。Ⅰ型AIP即IgG4相关性AIP,又称淋巴浆细胞硬化性胰腺炎(LPSP),病理表现:①大量浆细胞和淋巴细胞浸润,其中浆细胞每高倍视野可见大于10个IgG4阳性细胞,且IgG4/IgG大于40%;②独特的席纹状或漩涡状纤维化;③静脉周围淋巴细胞和浆细胞浸润导致闭塞性静脉炎。Ⅱ型AIP属非IgG4相关性胰腺炎,临床特征为胰腺体积增大,组织学无或极少见IgG4阳性浆细胞。血清IgG4>1350mg/L作为诊断的最佳截断值,其敏感性和特异性分别为97.0%和79.6%。此外,还应行全身PET扫描,明确是否累及胰腺外组织器官。
7.最终诊断
①自身免疫性胰腺炎Ⅰ型;②高血压;③2型糖尿病。
8.后续治疗方案
给予泼尼松治疗,初始剂量为30mg/d,疗程3~4周,以每1~2周减量2.5~5mg的速度逐渐减量,至每日5mg转为维持治疗,总疗程可达3年。
9.后续随访
治疗1个月后,磁共振检查与之前对比,提示胰头部结节影,胰体尾部肿大,范围较前缩小。
AIP的临床表现缺乏特异性,影像学描述提示该疾病的作用相当重要。AIP的超声表现为低回声胰腺实质内可见散在高回声区域,主胰管不规则狭窄,节段性病变通常表现为肿块型病灶,与胰腺癌的鉴别困难。对于难以鉴别的病例,可在服药2周后,通过血清学及影像学检查评估疗效,若疗效不佳,应将胰腺癌重新纳入考虑范围。
[1] 朱晓斐,邹多武. IgG4相关性消化疾病的研究进展. 中国胰腺疾病杂志,2014,14:57-61.
[2] 钱家鸣. 消化内科学. 2版. 北京:人民卫生出版社,2014.











