英文名称 :hypertensive intracerebral hemorrhage
中文别名 :高血压脑出血
高血压脑出血是由于高血压病伴发的脑小动脉病变在血压骤升时破裂所致,称为高血压性脑出血。其原发于脑实质,为非外伤性自发性出血,出血也可扩展至脑室或蛛网膜下腔。
每年全球200万~300万人发生脑出血,占所有新发脑卒中的10%~15%,脑出血全球总发病率为24.6/(10万·年)。在我国,脑出血发病率为60~80/(10万·年),该数据远远高于西方国家和其他亚洲国家。脑出血中原发性脑出血占80%~85%,原发性脑出血合并高血压者占50%~70%。尽管脑出血约占脑卒中发病的20%,但其致死和致残率却远高于后者。
高血压脑出血多按照出血部位分类,多灶性出血罕见。也有按发病时间将其分为特急性、急性和亚急性,或按病情轻重分为轻、中、重型。
高血压脑出血按部位分为基底节区出血、丘脑出血、皮层下脑叶出血,脑干(脑桥)出血和小脑出血,其中最多见的是基底节区出血,约占全部高血压脑出血的50%。出血位于幕下的约占20%~30%,可以发生在小脑半球、小脑蚓部和脑干,脑干出血主要发生在脑桥,大约占全部高血压脑出血的3%~13%。
有人又将基底节区出血细分为壳核型(血肿局限于壳核内),壳核-内囊型(血肿向内侵犯内囊),壳核进展型(血肿以壳核为中心向周围扩展,累及内囊、半卵圆中心、放射冠和部分颞叶及侧脑室)和脑室型(血肿巨大,破入侧脑室和第三脑室)等4型。将丘脑出血细分为丘脑型(血肿小,局限于丘脑内)、丘脑-内囊型(血肿向外侵犯内囊)、丘脑底-中脑型(血肿向下侵犯丘脑底部和中脑)和脑室型(向内破入脑室)等4型。
临床分型的目的是便于指导治疗和判断预后。天津马景鉴、杨树源等1995年按CT所见和患者预后提出将高血压脑出血分为幕上和幕下两大类,幕上出血占71%,又分为浅表型(壳核、外囊和皮层下)、深部型(基底节内侧、内囊、丘脑)和脑室型(血肿主要破入脑室),其中深部型占59%;幕下又分为外侧型(小脑外侧)、中间型(蚓部和脑干)和混合型(小脑外侧和蚓部),其中外侧型占45%。幕上的深部型和脑室型死亡率明显高于浅表型,幕下的中间型和混合型死亡率高于外侧型,为降低死亡率,前者在治疗上应考虑更为积极的外科干预。
根据出血后患者的意识状态,临床又将其分为五级,以便记录比较,并作为判断手术指征时参考。五级为:Ⅰ级清醒或嗜睡,伴有不同程度偏瘫和/或失语;Ⅱ级:嗜睡或朦胧,伴不同程度偏瘫和/或失语;Ⅲ级:浅昏迷,伴偏瘫,瞳孔等大;Ⅳ级:昏迷,伴偏瘫,瞳孔等大或不等大;Ⅴ级:深昏迷,去脑强直或四肢软瘫,瞳孔单侧或双侧散大。
高血压脑出血的发病原因是脑内小动脉在长期高血压刺激发生慢性病变基础上破裂所致。由颅内大动脉直接发出小动脉的直径约为100~200μm的穿通血管,包括豆纹动脉、丘脑穿通动脉以及基底动脉的脑干穿通支等。这些微小动脉的慢性病变主要包括脑小动脉硬化、脑血管透明脂肪样变性以及粟粒状微动脉瘤形成等。
粟粒状动脉瘤又称微动脉瘤,主要指脑内小动脉某些局部呈纺锤样扩张,好发于基底核、丘脑、脑干等部位,是高血压脑出血的可能原因。出血多在脑实质,出血到一定程度形成血肿。血肿形成后,随时间进展而呈现不同的病理特点。超急性期(6h内),血肿形成边缘多不规则,血肿内一般无脑组织。血肿周围血管充血,局部高压引起周围脑组织受压移位、缺血、水肿和坏死。急性期血肿周围脑水肿明显,半球体积增大,压迫该侧脑室变形并向对侧移位甚至形成脑疝,脑疝常为脑出血致死的直接原因。24h后局部出现白细胞浸润,血肿开始溶解,呈果酱状或渐渐液化,周围新生毛细血管形成,巨核细胞浸润,血肿液化后连同周围液化坏死的脑组织一起被由小胶质细胞和血管外膜来源的细胞所吞噬,血肿因而逐渐被吸收。血肿液在早期呈黑褐色,渐呈棕色,最后变成草黄色液体。血肿周围的胶质和结缔组织增生,上有含铁血黄素沉着而呈棕黄色。少数血肿可机化。
长期高血压病可导致小动脉壁透明样变性,内膜下脂质和蛋白质沉着,累及全身小动脉,尤其以心、肾、脑血管受影响最大。由于小动脉壁的病变导致强度下降,在长期高血压的作用下,脑底部的穿支动脉可发生大量粟粒状微小动脉瘤,又称Charcot-Bouchard动脉瘤。这些细小的穿支动脉直接自颅底的大动脉发出,承受的血压高于其他部位同等直径的小动脉,在突然升高的血压冲击下容易破裂出血。自从一百多年前Charcot和Bouchard发现脑底部穿支动脉的微小动脉瘤后,上述小动脉改变导致高血压脑出血的学说已被广泛接受,但是什么原因造成小动脉壁变性、内膜下脂质和蛋白质沉着,这种改变能否逆转和如何逆转的问题,至今尚未有满意的答案。最近有人将开颅血肿清除术时找到的出血动脉仔细取出做病理检查,发现部分高血压脑出血患者的出血动脉存在内膜剥离现象,并形成夹层动脉瘤,此类病变导致的动脉破裂约占高血压脑出血的20%。
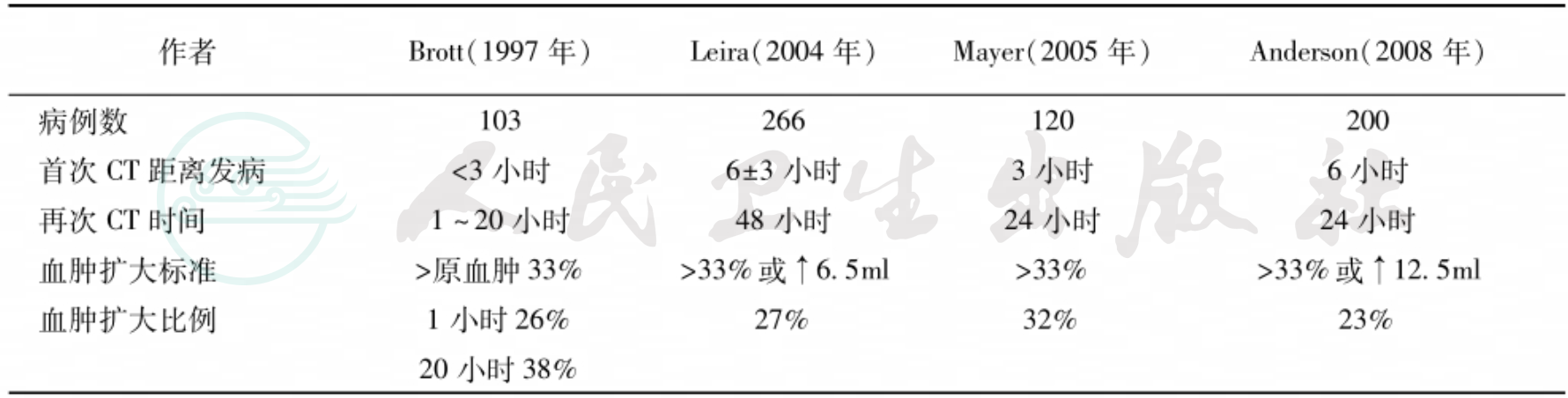
小动脉破裂出血后,血凝块释放的血管活性物质可以使动脉收缩,其周围的压力随着血肿量增加而升高,患者凝血机制无异常时,出血在数分钟到数小时后会自行停止,24小时后血肿通常不再继续增大。Kazui等分析了204例患者的CT影像,发现出血后3小时内血肿继续增大者占36%,6小时后占17%,但24小时后降至0。日本一组90例高血压脑出血,24小时内重复CT扫描,9例发现血肿增大。国内一组300例患者,早期血肿增大的为20.3%,其他一些报告见表1。总体上,脑出血后接受首次CT检查的时间越早,发现血肿扩大的概率就越高。血肿增大的原因多与出血后血压过高有关,而发病后经常出现的颅内压升高、频繁呕吐、呼吸道梗阻等均可导致血压升高。此外患者凝血机制障碍(如正在服用抗凝药物)、过度使用药物脱水等也可能导致血肿增大。如何预测早期血肿扩大,目前尚缺乏可靠方法,临床发病后患者症状不断恶化时,特别要考虑是由于出血未停止,血肿增大所致,应及时复查CT。文献报告对脑出血患者行CTA检查,如发现血肿内存在斑点样或线状增强,即“斑点征”(spot sign),可独立预测血肿将增大。脑内血肿早期增大的患者预后较血肿稳定者差。
表1脑内血肿发病早期扩大的部分报告
脑内血肿开始是暗红色的血凝块,沿白质纤维间隙扩张,数小时后略收缩变硬,不易吸除。周围脑实质受压缺血,可导致点片状坏死出血。此后的1~2周内血肿逐渐自溶,其内的血红蛋白在1~2天中自外向内逐渐由氧合血红蛋白转变为脱氧血红蛋白,其后数周到数月内在炎性细胞浸润作用下被分解吸收,遗留下胶质增生和含铁血黄素沉着,最终形成小的空腔。
脑内血肿占位效应及血肿在形成和降解过程中释放的生物活性物质,导致脑内发生一系列病理变化和器质性损害(图1)。

图1脑出血后的病理生理改变
出血量超过颅内有效代偿容积后,如不采取治疗措施干预,其病理过程将自然形成恶性循环,升高的颅内压使脑血流下降,缺血缺氧的脑组织发生代谢障碍和水肿,使颅内压进一步升高,病人情况进行性恶化,多在数天内死亡。出血量少时,仅影响局部脑组织,导致部分神经功能障碍,不形成致命的恶性循环,病人度过急性期后,脑水肿消退,血肿逐渐吸收,形成裂隙样空腔,周围胶质瘢痕增生。存活病人神经功能可以部分恢复,但多留下永久性损害
Suzuki和Ebina最早指出脑内血肿除占位效应外,还有毒性作用。Kanno等在大鼠脑神经元培养液中加入不同浓度的血红蛋白,24小时后检测神经元活性。发现神经元活性降低程度与血红蛋白浓度有关,高浓度血红蛋白对神经元有毒性作用。
脑水肿是脑损伤的重要表现,实验证实,由于凝血级联反应,凝血酶原激活转变为凝血酶,后者具有神经毒性作用,是导致脑水肿的主要原因。正常循环血液中不存在可以测出的凝血酶,但在脑出血后,通过凝血级联反应每毫升血浆可产生210~360U凝血酶,仅1U凝血酶就可使1ml血液在15秒内凝固。已证实由凝血酶原转变为凝血酶的程度与血肿周围脑水肿程度一致,并可被凝血酶抑制剂(如nexin-1蛋白酶、水蛭素)所抑制。有实验分别用全血或惰性油蜡混合物注入鼠脑,发现仅全血造成周围脑水肿。用微球囊模拟占位效应,可造成脑血流下降,但在头24小时内并无脑水肿出现。用猪脑出血模型试验,24小时内血块收缩,血肿体积变小,周围脑水肿反而明显,同时发现血肿周围血清渗出后1小时,即出现脑水肿。体外实验发现,凝血酶可抑制鸡和鸟的脊髓运动神经元,诱发其退变、死亡。在C6胶质瘤细胞培养液中加入凝血酶,24小时后标志脑细胞损伤的乳酸脱氢酶(LDH)明显增加,培养液中凝血酶≥500nmol/L时可致星形细胞和海马神经元死亡。
此外,动物实验及临床应用SPECT及PET观测结果表明,脑出血后血肿周边存在着脑血流量下降现象,其程度与血肿大小及部位有关,小量出血使局部血流短时下降,大量出血则可致同侧半球长时间缺血。丘脑出血引起的双侧半球血流下降较之壳核出血更明显,且持续时间长,表明出血部位越靠近中线,脑血流改变也越明显。缺血将导致脑组织细胞能量代谢障碍,ATP储备耗尽后,细胞膜的正常跨膜电位不能维持,钠离子、钙离子和水内流,兴奋性氨基酸释放,自由基生成,最终使细胞肿胀坏死。动物实验表明,当脑血流量下降到20ml/(min·100g)脑组织以下,脑的功能即受到损害,低于10~12ml/(min·100g)脑组织,2~3小时内即可发生脑组织梗死。正常成年人颅内代偿容积有限,幕上约为60ml,幕下15ml左右。大脑半球出血量﹤50ml时,对颅内压及脑灌注压的影响还是可逆的,如超出此耐受阈值,血肿占位和对脑组织的毒性作用造成的颅内高压和脑血流量下降将形成恶性循环,导致患者死亡。
经受住了脑出血急性期打击的患者,随着血肿的逐渐吸收,症状逐渐好转,进入延续1~2年的恢复期,多数患者最后会遗留或轻或重的神经功能障碍,仅少数出血量少,或出血部位在非重要功能区的患者可以完全恢复。
(一)计算机断层扫描(CT)
头部CT是最重要的辅助检查手段。在CT设备已经普及的今天,对怀疑有脑出血的患者应立即行常规头部CT扫描。初发病时脑内血肿在CT平扫上呈现明显的不规则片状高密度影(CT值约28~45Hu),边缘清晰,与周围的脑组织(CT值约15~27Hu)极易区别。数小时后,血肿周围脑组织水肿可出现低密度区,脑内结构受压移位。4~7天后血肿的密度逐渐减低(每天降低约2Hu),2~3周后血肿的CT值与脑组织相同,此时不要误以为血肿已吸收(图2~图4)。CT检查可以迅速明确诊断,确定出血部位并计算出血肿体积,必要时还可以重复检查,动态观察血肿变化。在常规CT片上也可以用改良的椭圆体体积公式(血肿体积≈血肿长径×宽径×高径/2)简单地估计血肿体积。准确掌握血肿的部位、大小、脑组织水肿和脑结构移位程度,对于决定下一步应采取的治疗措施和判断患者预后帮助极大。
原发性单纯脑室出血甚为少见,临床上多数(>80%)为脑室附近实质内出血破入脑室,依序为:底节、丘脑、小脑、脑桥。脑室出血后,如脑室液中血细胞比容>16%,CT片上才能表现为出血,如<12%则不能提示。此外,脑室液CT值为20~40Hu提示为血性脑室液,40~80Hu则为血凝块。
多层螺旋CT动脉血管成像技术(CTA)可以显示脑内主要血管影像,排除血管畸形,有助于判断破裂出血动脉的部位及是否有活动出血,预估血肿继续扩大的可能性。

图2典型壳核出血的CT图像,可见血肿将内囊向内推挤,并破坏部分内囊进入苍白球并破入侧脑室

图3图2患者经小切口“锁孔”开颅血肿清除术后1天,CT复查可见直径约2.5cm的骨窗及脑内的引流管影,血肿清除满意,脑室移位已基本恢复,但脑内和脑室内仍可见积血
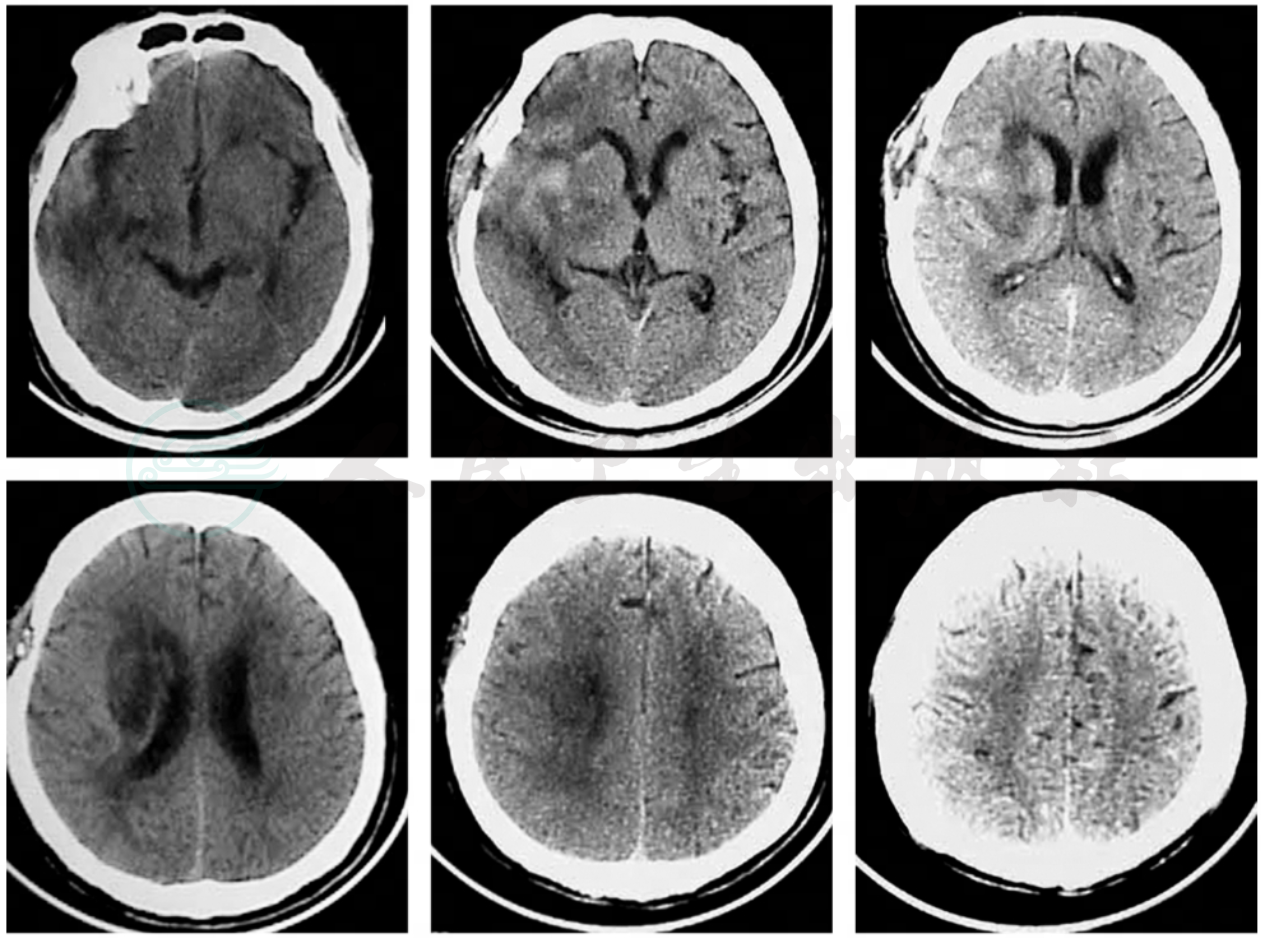
图4同一病人手术后15天,脑内血肿已消失,脑室及中线结构已恢复正常位置
(二)脑血管造影
脑血管造影通常极少能直接看到造影剂溢出破裂动脉,也不能显示血肿本身,本身有一定风险,且耗时费力,但在脑出血的鉴别诊断上脑血管造影仍然有不可替代的作用。对不典型的自发性脑出血,怀疑有脑血管畸形或动脉瘤破裂的患者,除可采用CTA外,必要时应考虑行脑血管造影(DSA)明确诊断。
(三)磁共振扫描
不同时期的脑内血肿在磁共振(MRI)扫描影像上有不同的特点,详见表2。MRI可以满足高血压脑出血的诊断要求,根据脑内血肿在MRI影像上的特点,还可以大致判断出血的时间,是否有反复多次的出血等。但MR检查需要患者较长时间(10分钟以上)静止不动地躺在扫描机内,这对已有意识障碍的患者很难做到。由于CT可以快速准确地做出脑出血的诊断,完全能够满足临床治疗的需要,价格也比MR低很多,因此一般不用MRI作为脑出血患者的首选检查,仅在患者度过脑出血急性期后,诊断上有疑问,需要进一步查明出血原因时,才考虑选用MRI检查。
表2脑出血不同时期影像学检查的表现

(四)其他
在不具备以上检查条件时,既往曾用颅脑超声检查以发现可能存在的中线结构移位,但准确性差,早已废用。血肿破入脑室或蛛网膜下腔时,腰穿脑脊液可以呈血性或红细胞计数升高,有助于脑出血和脑梗死的鉴别。CT已明确诊断的患者,无须再行腰穿检查。











