英文名称 :acute myocardial infarction
中文别名 :心梗
AMI是指由于冠状动脉急性狭窄或闭塞,供血持续减少或终止,所产生的心肌严重缺血和坏死。其主要病理生理机制是在冠状动脉粥样硬化的基础上,由于某些机械原因(如高血压或冠状动脉痉挛等)诱发了易损性斑块(vulnerable plaque)破裂和血栓形成,导致急性冠状动脉严重狭窄或完全闭塞的结果。
AMI在中、老年多发,男性多于女性,亦可见于青年人;近年来在我国发病“年轻化”、“老年化”和“农村化”的趋势明显。AMI起病急,发病凶险,病死率高,预后差,是冠心病极其危重的表现类型。AMI的主要死因为室性心律失常(主要是心室颤动)、泵衰竭和机械并发症等,发病后12小时内因室颤而死亡者约占总死亡者的一半,发病后6小时内若不能有效地使梗死相关冠状动脉再通,则大面积(>40%)梗死者多会并发泵衰竭,包括心源性休克和左心功能衰竭,存活者多数演变成慢性心力衰竭,也是冠心病心力衰竭形成的主要原因。对晚期(12~24小时)再灌注治疗者,因机械并发症和再灌注治疗本身并发症致死也并不少见。可见,AMI是心血管疾病中最危重的紧急事件,临床表现多样,危重程度不一,病情变化迅速,治疗措施关键,需要及时、准确地诊断和正确地抢救治疗,也是对心内科医生临床综合诊治水平和技能的挑战。
尽管近十年来国内外AMI指南不断更新,主要是为其治疗原则提供循证医学证据,有重要的临床指导作用,然而丝毫不能替代临床医生对每位AMI患者个体实施的优化治疗,以挽救患者生命,改善近远期预后。
AMI根据心电图(ECG)表现传统上分为Q波型和非Q波型,并对应病理上透壁和非透壁性(又称心内膜下)心肌梗死(MI);近年来又结合冠状动脉病理生理改变则统一称之为ST上抬型和非ST上抬型MI(STEMI和NSTEMI),前者提示冠状动脉急性完全闭塞,后者是由于冠状动脉未完全闭塞或闭塞后迅速再通或有侧支循环替代的结果。在此基础上,欧美心脏病协会(2007年)又根据不同病理生理机制和临床表现将AMI“分门别类”地分为Ⅰ(冠状动脉原发血栓性)、Ⅱ(非血栓性)、Ⅲ[猝死(sudden cardiac death,SCD)性]、Ⅳ(介入相关性)和Ⅴ(冠状动脉旁路移植术后)5个类型,其中Ⅳ型又分为Ⅳa(介入后冠状动脉栓塞、分支闭塞所致)和Ⅳb(支架内血栓)两个亚型。
一、冠状动脉易损斑块破裂
AMI的病理基础虽说是传统认识的冠状动脉粥样“硬化斑块”,然而实际上是粥样“软化斑块”,即“易损斑块”(vulnerable plaque)或“不稳定斑块”,其破裂诱发血栓形成是AMI的重要病理生理基础。
二、冠状动脉急性血栓性狭窄或闭塞
冠状动脉内易损斑块一旦破裂,暴露出内皮下胶原,血小板立即由vWF(von Willebrand factor)介导其黏附(adhesion)、激活(activation)和聚集(aggregation)反应,形成血小板血栓(即白血栓);后以聚集血小板的磷脂为基础,迅速激活凝血瀑布,使凝血酶原生成凝血酶,催化纤维蛋白原为纤维蛋白,“网络”红细胞形成红血栓,使冠状动脉管腔产生急性狭窄或闭塞,致临床上突发急性冠状动脉综合征(acute coronary syndromes,ACS)。
若冠状动脉完全闭塞,临床上则表现为典型的STEMI,若未完全闭塞或短暂闭塞后又再通,临床则表现为NSTEMI或不稳定型心绞痛,前者心肌缺血时间长(>20分钟),后者时间短(或<20分钟或一过性)。血小板激活同时,又释放血栓素(thromboxane A2,TXA2)和二磷酸腺苷(ADP),正反馈促发自身激活和聚集(纤维蛋白原与血小板糖蛋白(GP)Ⅱb/Ⅲa受体结合介导),促进血栓形成。可见,抗血栓治疗是AMI防治的基础。
三、心肌缺血和坏死
冠状动脉急性狭窄或闭塞的直接结果是导致心肌缺血或坏死,通常由心内膜下波面扩向心外膜下。缺血或坏死范围的大小取决于冠状动脉供血范围、减少的程度和时间以及有无侧支循环形成。
病理上,AMI可分为透壁性和非透壁性(或心内膜下)梗死。前者心肌梗死累及左心室壁全层,多由冠状动脉持续闭塞所致;后者坏死仅累及或局限于心内膜下,多是冠状动脉急性狭窄或短暂闭塞而又持续再通或伴侧支循环迅速开放的结果。第三种情况为部分非透壁梗死从内膜下累及约1/2心室壁层,多见于STEMI在未形成透壁梗死前,早期冠状动脉自发或治疗性成功再通并使心肌得以成功再灌注的患者。
AMI的病理生理特征是由于心肌丧失收缩功能所产生的左室收缩功能降低、血流动力学异常和左心室重构,心肌再灌注损伤、无再流以及修复和再生。
一、左室收缩功能降低
AMI后3~5分钟内,梗死区心肌很快丧失收缩功能而产生左室受累节段收缩功能减弱或消失。临床上则表现为不同程度的泵衰竭,即左心衰竭、肺水肿,甚至心源性休克。左室整体收缩功能降低的程度取决于MI面积的大小和左室节段运动异常的范围。若MI面积>40%,则临床上会产生心源性休克,若节段运动异常的范围>25%,则临床上可出现左心衰。
二、血流动力学异常
AMI患者左室节段、整体收缩和舒张功能下降的同时,即产生特征性的血流动力学异常:每搏输出量(SV)、心排血量(CO)降低和左室舒张末压(LVEDP)异常升高。前者主要影响前向动脉供血,致血压和组织灌注降低;后者则引起后向淤血,致肺淤血或肺水肿;两者综合在临床上表现为不同程度的左心衰竭,严重时出现急性肺泡性肺水肿和心源性休克。AMI的血流动力学异常程度也取决于心肌梗死和缺血范围的大小和左室收缩功能降低的程度。
1967年,Killip等根据AMI患者的临床表现所提出的心功能分级(Killip Ⅰ~Ⅳ级,分别代表正常、轻、中和重度心衰和心源性休克)就已较好地反映出上述不同程度的血流动力学异常。1976年,Swan、Forrester利用Swan-Ganz右心漂浮导管对AMI患者进行血流动力学监测,根据所测CO,计算出CI(心输出指数)和反映LVEDP的肺毛细血管楔压(PCWP),将AMI的血流动力学分为以下四种类型:
Ⅰ型,正常型,即CI[>2.2L/(min·m2)]和PCWP(≤18mmHg)均在正常范围,组织灌注正常,也无肺淤血。
Ⅱ型,肺淤血、水肿型,即CI正常[>2.2L/(min·m2)],仅PCWP升高(>18mmHg),组织灌注正常,仅有肺淤血、肺水肿。
Ⅲ型,组织低灌注型,即CI[≤2.2L/(min·m2)]降低,但PCWP正常(≤18mmHg),仅有组织低灌注,但无肺淤血。
Ⅳ型,心源性休克型,既有CI降低[≤2.2L/(min·m2)],又有PCWP升高(>18mmHg),临床既有组织低灌注,又有肺水肿的典型心源性休克表现。这一经典分型,对于临床正确估测AMI患者血流动力学状态和预后,指导临床正确治疗具有重要的意义。
三、左心室重构和扩大
AMI致左室节段和整体收缩、舒张功能降低的同时,机体就迅速激活了交感神经系统、肾素-血管紧张素-醛固酮系统(RAS)和Frank-Starling等代偿机制,一方面通过增强非梗死节段的收缩功能、增快心率代偿性增加已降低的SV和CO,并通过左室壁伸长和肥厚增加左室舒张末容积(LVEDV)进一步恢复SV和CO,降低升高的LVEDP;但另一方面,也同时启动了左心室重构和扩大的过程。
AMI左室重塑(LV remodelling)是指AMI后所产生左室大小、形状和组织结构的变化过程,亦即梗死区室壁心肌的变薄、拉长,产生“膨出”即梗死扩展(infarct expansion)和非梗死区室壁心肌的反应性肥厚、伸长,致左室进行性扩张和变形伴心功能降低的过程。AMI左室重塑与临床上产生心脏破裂、真(假)室壁瘤形成等严重并发症和心脏扩大、心力衰竭有关,是影响AMI近、远期预后的主要原因之一。
因此,积极防治AMI左室重塑对于预防严重并发症和心力衰竭发生,进一步改善AMI患者的近、远期预后均有着重要的临床意义。AMI左室重塑的有效干预措施包括:①早期(<6小时)再灌注治疗包括溶栓和急诊PCI;②晚期(>6小时而<24小时)冠状动脉溶栓再通、补救性PTCA和延迟性或恢复期PCI;③血管紧张素转化酶抑制剂(ACEI)、血管紧张素受体拮抗剂(ARB)、硝酸酯类和β受体阻断药;④避免使用糖皮质激素和非甾体抗炎药。
四、心肌缺血再灌注损伤
心肌缺血再灌注损伤是指AMI冠状动脉开通治疗成功,缺血心肌再获血供(即再灌注)后损伤反而加重甚至进一步坏死现象。临床意义是尽管AMI再灌注治疗成功,然而梗死范围并未缩小,心功能和预后依然差,是AMI再灌注治疗的难题。
五、冠状动脉和心肌无再流现象
冠状动脉和心肌无再流现象是指AMI再通治疗成功,开通闭塞的冠状动脉后,冠状动脉仍无或慢血流现象(no-reflow或slow-flow phenomenon),是再灌注治疗时代不能实现心肌有效再灌注的主要原因,直接后果是心肌进一步缺血性坏死、梗死范围扩大和预后差。
六、心肌修复和再生
AMI患者心肌坏死后,细胞自然开启了修复过程,主要是坏死心肌溶解、吸收、由成纤维细胞分泌胶原修复和瘢痕组织形成。这一病理性过程需要4~6周时间。近期研究发现,在梗死心肌修复过程中,同时有心肌和血管再生参与其中,主要机制是动员血液中骨髓内皮祖细胞、间充质干细胞归巢到梗死区和心脏本身的心肌干细胞自行再生来完成。这也奠定了近年来干细胞治疗AMI研究的理论和实践基础。
一、心电图变化
ECG是最为方便和普及的检查和诊断AMI的必备依据之一,又有其特征性改变和动态演变,故临床上只要疑有AMI,就必须尽快记录一张12导联或18导联(加做V7~V9和V3R~V5R)ECG以确定或除外AMI的诊断。
AMI时,心肌缺血(ischemia)、损伤(injury)和梗死(infarction)在ECG相应导联上,分别特征性地表现为ST段压低或T波的高尖或深倒、ST段的上抬和Q波的形成。
AMI超急性期,即冠状动脉全闭塞伊始,ECG相应导联随即出现短暂的高尖T波,接下来很快进入急性期而出现ST段上抬,伴对侧导联ST段镜向性压低这一冠状动脉急性闭塞致AMI的特征性变化,1~2小时后由于心肌坏死而渐出现病理性Q波和R波消失。
因此,在AMI早期数小时内,ECG的典型改变是相应导联异常Q波、ST段上抬和T波的直立或浅倒。偶见T波高尖或深倒,提示冠状动脉刚刚发生急性闭塞或闭塞后已有再通。
然而,ECG对AMI最具诊断价值的特征性改变是其“动态演变(evolution changes)”,即AMI发病后数小时、数天、数周,个别数月中,在ECG上有一个特征性的动态演变过程:抬高的ST段迅速或逐渐回复到等电位线;同时伴相应导联Q波的形成并加深、加宽,R波的降低和消失,呈现典型的QS波形;T波从短暂高尖到自ST段末端开始倒置并渐渐加深至深倒呈对称的“冠状T”,然后又渐渐的变浅和直立。ECG若呈这一“动态演变”过程,则可确诊为AMI;无动态演变则可除外诊断,如早期复极综合征和恒定不变冠状T的心尖肥厚型心肌病。另外新出现的完全左束支阻滞(CLBBB)也是AMI特征性改变,提示发生了AMI且预后差。广泛前壁AMI患者出现完全右束支阻滞(CRBBB)者,提示梗死范围大、坏死程度重和预后差。
ECG对AMI的定位诊断依据不同部位导联的特征性变化和动态演变。前壁导联(V1~V4)、侧壁导联(V4~V6)、高侧壁导联(Ⅰ、aVL)、下壁导联(Ⅱ、Ⅲ、aVF)、正后壁导联(V7~V9)加上RV导联(V3R~V5R)的变化就诊断为该部位AMI。在新出现的CLBBB时,则是前壁AMI。
AMI均是由于冠状动脉急性闭塞所致,故冠状动脉闭塞与ECG梗死部位有明确的对应关系如下:冠状动脉前降支(LAD)闭塞,引起前壁+高侧壁AMI;左旋支(LCX)闭塞可引起下壁伴前侧壁、高侧壁或正后壁AMI,其开口部闭塞偶呈前壁心肌梗死改变;右冠状动脉(RCA)闭塞可引起下壁、正后壁、侧壁和RV的AMI;左主干(LM)闭塞产生LAD+LCX都闭塞的广泛心肌缺血和梗死。重要的是,不同冠状动脉闭塞和相同冠状动脉不同部位闭塞所产生的AMI范围大不相同。就右优势型不同冠状动脉闭塞而言,梗死范围从大到小依次为LM>LAD>RCA>LCX,左优势型冠状动脉时RCA闭塞时,理论上只产生单纯右室梗死,左心室无梗死;而相同的冠状动脉而言,三大主支近端闭塞梗死范围大,主支远端和分支闭塞则范围小,左主干闭塞(3%~5%)的缺血和梗死范围最大,可随时因心血管崩溃(cardiovascular collapse)而死亡。
二、实验室检查
1.心肌损伤标志物
AMI后,随着心肌细胞坏死和细胞膜的完整性破坏,心肌细胞内的大分子物质即心肌损伤标志物(心肌酶和结构蛋白)开始释放入血,使血中浓度有一异常升高和恢复正常过程,也是临床上诊断AMI的必需依据。目前,临床最常用的心肌标志物包括肌酸磷酸激酶(CPK)或肌酸激酶(CK)及其同工酶MB(CK-MB)、肌红蛋白、肌钙蛋白T或I(cTnT或cTnI)、乳酸脱氢酶(LDH)和同工酶LDH1等。
这些酶一般在AMI发病后4~8小时在血中开始异常升高,平均24小时达峰值,2~3天内降至正常水平。只是肌红蛋白升高和峰值提前至12小时;cTnT或cTnI峰值更后,持续时间更长,理论上1~2周才消失,可为晚期AMI(早期已误诊者)诊断提供证据;近年研发的高敏肌钙蛋白T或I(hs-cTnT或cTnI)可在AMI后3~4小时血中就升高,对早期诊断优势也突出。
为提高对AMI诊断的准确率,临床一般在发病后8~10小时、20~24小时和48小时连续多时间点取血,并检测多个心肌酶谱或组合,观其动态变化,以综合判断。单一CK和CK-MB升高,可见于剧烈运动、肌肉损伤、肌肉按摩和甲状腺功能低下者,此时心肌结构特有的cTnT或cTnI正常。AMI诊断时常规采用的血清心肌标志物及其检测时间(表1)。
表1 AMI的血清心肌标志物及其检测时间
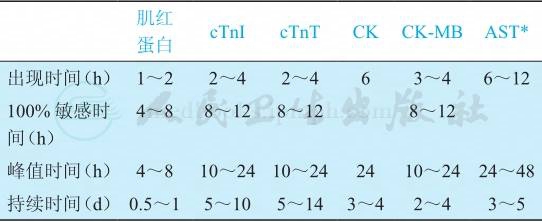
注:*应同时测定丙氨酸转氨酶(ALT),AST>ALT方有意义;CK:肌酸激酶;CK-MB:肌酸激酶同工酶;AST:天冬氨酸转氨酶。
2.其他实验室检查项目
包括血常规、肝肾功能、血脂血糖、出凝血时间和血气等项检查,是常规,然而多不作诊断之用。
三、影像检查
1.床旁X胸片
AMI时能准确评价有无肺淤血和肺水肿存在、消退情况和心影大小,对诊断心衰肺水肿有不可替代的重要价值。
2.床旁超声多普勒心动图
能检出梗死区室壁节段运动减弱、消失、矛盾动运,甚至膨出,还能评价整体收缩功能和心内结构、心包情况,对AMI及其并发症,特别是机械并发症的诊断和鉴别诊断有重要价值。应特别注意的是,在STEMI患者,切不可因等待此项检查和结果而延误早期再灌注治疗的时间。
3.核素心肌灌注显像
虽可检出梗死区充盈缺损,对诊断AMI有确诊价值,但不作为常规检查。
4.心血管CT或MRI
对AMI诊断和鉴别诊断有价值,只在特殊情况下如疑有大动脉夹层和急性肺栓塞时才应用。
AMI患者经CCU监护救治使病情稳定后,应转至普通病房进一步恢复,彻底检查,调整治疗和给予健康宣教后方可出院,时间1~2周。其间,除了延续和调整CCU的治疗方案外,还需完成上述相关检查的复查,以了解病情或心功能恢复情况;有条件还可做放射性核素心肌灌注检查,评价梗死范围大小;病情平稳后,还应当常规行冠状动脉造影和左室造影检查,在明确冠状动脉解剖病变和心功能状态后,进一步行PCI或CABG以及少数患者干细胞治疗。
此后,只要其生命体征稳定,能常规下地活动,生活自理,完成了健康宣教,并符合常规PCI术后出院条件时,即可出院。对AMI患者可喻为“心脏发动机”的突发故障者,应当进行彻底检查和治疗,以使其达到“心脏发动机和供油管道”理论上均彻底恢复的目的,使患者有机会重新恢复工作和生活。











