英文名称 :pulmonary edema
肺水肿(pulmonary edema)是指肺血管外水份的渗出或漏出的速度超过淋巴回流量,导致肺泡腔内液体聚积。产生的原因很多,包括肺内源性和肺外源性。临床主要表现为发绀、咳嗽、气促、气喘、咳粉红色或血性泡沫痰,听诊两肺散在细湿啰音,有时会有哮鸣音,胸部X线片可表现为以肺门为中心的蝶状或片状模糊阴影。深入理解肺泡上皮细胞液体转运机制,有助于诊断和治疗肺水肿。
无肺泡液体清除时,调控液体跨肺泡上皮屏障转运的各种因素可通过Starling公式来概括,同时考虑到滤过面积和回收液体至血管内的机制时,可改写为下面公式:
EVLW={(SA×Lp)[(Pmv-Ppmv)-σ(πmv-πpmv)]}-Flymph
式中EVLW为肺血管外液体含量;SA为滤过面积;Lp为水流体静力传导率;Pmv和Ppmv分别为微血管内和微血管周围静水压;σ为蛋白反射系数;πmv和πpmv分别为微血管内和微血管周围胶体渗透压;Flymph为淋巴回流量,概括了所有将液体从肺泡腔内转运到血管内的生理机制。
该公式表明,如果SA、Lp、Pmv和πpmv部分或全部增加,其他因素不变,EVLW即增多。Ppmv、σ、πmv和Flymph的减少也产生同样效应。由于重力和肺机械特性的影响,肺内各部位的Pmv和Ppmv并不是均匀一致的。在低于右心房水平的肺区域中,虽然Pmv和Ppmv均可升高,但前者的升高大于后者升高的程度,这有助于解释为什么肺水肿易首先发生在重力影响最明显的部位。
正常时肺间质和肺泡均能保持理想的湿润状态,这是由于淋巴系统、肺间质蛋白和顺应性的特征有助于对抗液体潴留,并连续不断地清除肺内多余的水分。肺血管静水压力和通透性增加时,淋巴流量可增加10倍以上对抗肺水肿的产生。起次要作用的是肺间质内蛋白的稀释效应,它由微血管内静水压力升高后致使液体滤过增多引起,效应是降低πpmv,反过来减少净滤过量。
肺泡Ⅱ型细胞在儿茶酚胺依赖性和非依赖性机制的调节下,可主动清除肺泡内的水分,改善肺水肿。Ⅰ型及Ⅱ型Na+通道的活性与肺泡内液体的清除率有关,某些疾病引起的Na+通道失衡会导致肺泡内液体清除受损,从而导致肺水肿的发生。据此,可以推论肺水肿的发病机制除了为Starling公式中包含的因素外,还受肺泡上皮液体主动转运功能的作用。只有液体漏出的作用强于回吸收的作用,并超过了肺泡液体的主动转运能力后才发生肺水肿。而且,肺泡液体转运功能完整也有利于肺水肿的消散。
肺泡表面总面积相当于一个篮球场大小,其中约有90%的肺泡表面被扁平Ⅰ型肺泡上皮细胞覆盖,其余10%的面积为Ⅱ型肺泡上皮细胞覆盖(图1)。Ⅱ型肺泡上皮细胞含有丰富的磷脂类物质,主要成分是二软脂酰卵磷脂,其分泌物在肺泡表面形成减低肺泡表面张力的肺泡表面活性物质,维持肺泡开放,并有防止肺泡周围间质液向肺泡腔渗漏的功能。这两种上皮细胞表面都含有钠离子通道,参与钠离子跨膜运输。钠离子先通过肺泡腔侧的阿米洛利敏感性钠通道进入细胞内,再由位于基底膜侧的Na+/K+-ATP酶将钠泵入肺间质。肺毛细血管内衬着薄而扁平的内皮细胞,内皮细胞间的连接较为疏松,允许少量液体和某些蛋白质颗粒通过。支气管肺泡上皮还表达3种特异性水转运蛋白(又称为水通道蛋白,aquaporin,AQP)——AQP1、AQP4、AQP5,可加速水的转运,参与肺泡液体的交换。
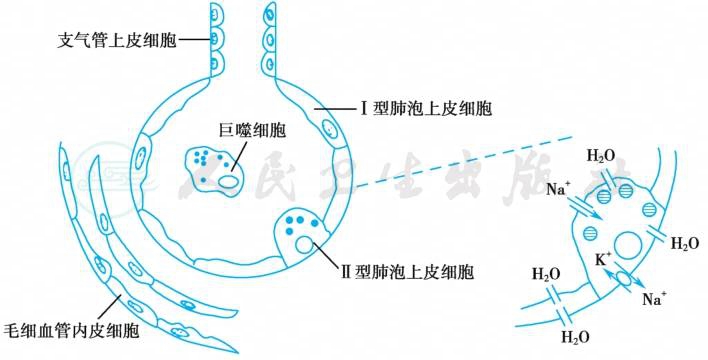
图1 肺泡液体交换形态学基础示意
电镜下可见肺泡的上皮与血管的基底膜之间并不完全融合,与毛细血管相关的肺泡壁存在一侧较薄和一侧较厚的膜(图2)。薄侧上皮与内皮的基底膜相融合,含肺泡上皮、基底膜和毛细血管内皮,有利于血与肺泡的气体交换。厚侧由肺毛细血管内皮层、基底膜、胶原纤维和弹力纤维交织网、肺泡上皮、极薄的液体层和表面活性物质层组成。上皮与内皮基底膜之间被间隙(肺间质)分离,该间隙与支气管血管束周围间隙、小叶间隔和脏胸膜下的间隙相连通,以利于液体交换。进入肺间质的液体主要通过淋巴系统回收。在厚侧肺泡隔中,电镜下可看到神经和点状胶原物质组成的感受器。当间质水分增加,胶原纤维肿胀刺激“J”感受器,传至中枢,反射性使呼吸加深、加快,引起胸腔负压增加,淋巴管液体引流量增多。
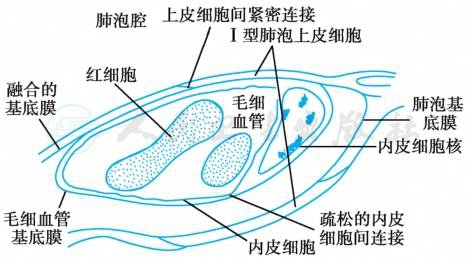
图2 肺泡毛细血管结构示意
为便于指导临床诊断和治疗,可将肺水肿分为高压性肺水肿(微血管压升高性)、常压性肺水肿(微血管压正常性)、负压性肺水肿(胸腔内和/或跨肺负压的绝对值增大)和混合性肺水肿(高微血管压合并高肺毛细血管膜通透性肺水肿)4类(表1)。
表1 肺水肿分类

肺表面苍白,含水量增多,切面有大量液体渗出。显微镜下可将其分为间质期、肺泡壁期和肺泡期。
间质期是肺水肿的最早表现,液体局限在肺泡外血管和传导呼吸道周围的疏松结缔组织中,支气管、血管周围腔隙和叶间隔增宽,淋巴管扩张。液体进一步潴留即进入肺泡壁期,液体蓄积在厚的肺泡毛细血管膜一侧,使肺泡壁进行性增厚。发展到肺泡期时,充满液体的肺泡壁会丧失其环形结构,出现褶皱。
肺水肿可影响肺顺应性、弥散、通气血流比例和呼吸类型,间质期最轻,肺泡期最重。肺含水量增加和肺表面活性物质破坏,可降低肺顺应性,增加呼吸功。间质和肺泡壁液体潴留,可加宽弥散距离。肺泡内部分或全部充满液体,可引起弥散面积减少和通气血流比例降低,产生肺泡动脉血氧分压差增加和低氧血症。
此外,肺水肿间质期即可表现出对血流动力学的影响。间质静水压升高,可压迫附近微血管,增加肺循环阻力,升高肺动脉压力。低氧和酸中毒还可直接收缩肺血管,进一步恶化血流动力学,加重右心负荷,引起心功能不全。
神经源性肺水肿(neurogenic pulmonary edema,NPE)是指无心、肺、肾等疾病的情况下,由中枢神经系统损伤导致的急性肺水肿。神经源性肺水肿存在两个可能的发病机制:一为循环动力学学说,二为肺血管通透性学说。同时,脑组织受损引起的儿茶酚胺大量释放、激活并释放大量炎症因子,进一步增加肺毛细血管通透性,更加剧了肺水肿。
负压性肺水肿(negative pressure pulmonary edema,NPPE)是一种因急性上呼吸道梗阻、试图用力吸气所产生的胸腔内或跨肺负压的绝对值增大导致肺泡-毛细血管损伤而引发的非心源性肺水肿。NPPE的病理生理学变化包括三个方面:①胸腔内高负压产生导致心脏前负荷增加,静脉回流增加,右心前负荷增加,进而引起肺动脉高压。②体循环血压增加引起心脏后负荷增加,上呼吸道梗阻时,缺氧刺激儿茶酚胺大量释放,使体循环血管收缩、外周总阻力增加,左室后负荷增加,左室功能不全。③肺泡-毛细血管屏障破坏,胸腔内或跨肺负压的绝对值增大可导致毛细血管内皮屏障断裂、肺泡上皮屏障断裂。机械通气时,由于呼吸设置不当或者镇静不够时,呼吸窘迫也会导致负压性肺水肿。
混合性肺水肿(comprehensive pulmonary edema)是多种因素引起的肺水肿。ARDS是典型类型,是因炎症反应导致的肺毛细管血管上皮屏障和肺泡上皮屏障破坏。
高压性肺水肿体检时可发现心脏病体征,临床表现依据病程而变化。在肺水肿间质期,患者可主诉咳嗽、胸闷、呼吸困难,但因为水肿液大多局限在间质腔内,只表现为轻度呼吸浅速,听不到啰音。因弥散功能受影响或通气血流比例失调而出现动脉血氧分压降低。待肺水肿液体渗入到肺泡后,患者可咳白色或血性泡沫痰,严重呼吸困难和端坐呼吸,可听到两肺满布湿啰音。血气分析提示低氧血症加重,甚至出现CO2潴留和混合性酸中毒。
负压性肺水肿的患者通常伴有急性呼吸道堵塞,呼吸困难,出现吸气时三凹征,患者面部表情痛苦、情绪激动,咳粉红色泡沫痰等。随着肺水肿进展,还可闻及肺部湿啰音,偶有哮鸣音。检查示氧饱和度进行性降低、严重的低氧血症等。
常压性和混合性肺水肿的临床表现可因病因而异,而且同一病因引起的肺水肿也可依不同的患者而呈现不同的临床表现。











