英文名称 :chronic kidney disease
慢性肾脏病(chronic kidney disease,CKD)已成为世界性的公共健康问题,随着人们生活水平的提高以及寿命的延长,CKD的发病率和死亡率有增无减。CKD患者最终会进展至终末期肾病(end stage renal disease,ESRD),需要长期依赖透析或肾移植维持生命,不仅严重降低患者的生活质量,也给社会和家庭带来了沉重的经济负担。
CKD的病因在西方国家以继发性因素为主,糖尿病和高血压为两大首位病因。我国CKD病因仍以IgA肾病为主的原发性肾小球肾炎最为多见,其次为糖尿病肾病、高血压肾损害、狼疮性肾炎、梗阻性肾病、多囊肾等。尽管中国的糖尿病和高血压在过去的15~20年呈现迅速增长趋势,但是目前对中国CKD人群构成的影响还需要大约10年的时间。
2012年一项流行病学研究调查了中国13个省市4.7万余人群,发现中国CKD的患病率是10.8%,2015年中国肾脏疾病监测网络(China Kidney Disease Network,CK-NET)数据显示,全国住院患者中CKD的发病率约为4.8%,合并有糖尿病和高血压的患者其CKD的发病率更是高达13.9%和11.3%,且CKD占比随着年龄的增长而增加。
CKD患者的肾脏损伤往往持续进展,导致肾单位和肾功能不可逆的丧失,最终导致ESRD,其致病机制复杂,至今仍未阐明。除原发病因、各种肾脏疾病特异性的病理生理改变之外,还存在一系列共同机制,包括肾小球高滤过、矫枉失衡、肾小管高代谢、蛋白尿、尿毒症毒素等学说。此外,各种生长因子和血管活性物质在CKD进展中的作用越来越被认识。
(一)肾小球高滤过学说
1986年Brenner等证实,健存肾单位存在肾小球滤过率增高(高滤过)、血浆流量增高(高灌注)和毛细血管跨膜压增高(高压力),即著名的“三高学说”或“肾小球高滤过学说”,其机制主要是残余肾单位入球小动脉较出球小动脉扩张更加显著所致。在三高状态下,肾小球显著增大,进而牵拉系膜细胞,使细胞外基质(extracellular matrix,ECM)大量积聚,会进一步加重肾小球损伤,最终发展为不可逆的肾小球硬化。
(二)矫枉失衡学说
慢性肾衰竭时体内某些物质的积聚,并非全部由于肾脏清除减少所致,而是机体为了纠正代谢失调的一种代偿适应,其结果又导致新的不平衡。CKD患者对钠平衡的维持就是一个典型。在肾脏损伤早期钠排泄减少,导致钠及细胞外液潴留,血压升高,早期的高血压有助于增加肾小球滤过及钠的排泄,然而这种维持钠平衡的矫枉失衡终将导致容量依赖性高血压。CKD进程中出现的钙、磷代谢异常也存在矫枉失衡的现象,但是该代偿机制的不良后果是产生了继发性甲状旁腺功能亢进症(继发性甲旁亢)、肾性骨病、心血管疾病等多系统病变。
(三)肾小管损伤学说
在CKD进程中,肾小管上皮细胞发生了炎症反应以及上皮细胞向间充质细胞的转分化过程(epithelial-mesenchymal transition,EMT),随之产生多种生物活性分子,导致间质炎症和纤维化。肾小管上皮细胞上的天然免疫受体也会加重免疫反应引起的坏死性炎症。最新研究发现,烟酰胺腺嘌呤二核苷酸(NAD+)依赖的肾小管代谢失衡也可能导致慢性肾脏病,进一步了解影响NAD+的生物合成可能为CKD的预防和治疗提供新的途径。
(四)高血压
持续高血压可导致肾功能减退,而肾功能进行性下降可导致血压难以控制,高血压与CKD之间的因果关系有时很难确定,大量循证医学证据表明血压的良好控制明显延缓CKD进展。高血压导致肾功能进行性下降的原因包括:首先,恶性高血压损伤入球小动脉及肾小球内皮细胞,甚至导致血管栓塞,直接造成肾功能下降;其次,高血压引起肾小球缺血性损伤,引起肾功能进行性减退。
(五)蛋白尿
研究表明,蛋白尿不仅仅是肾小球疾病最常见的临床表现之一,而且是一个独立的导致肾脏病变进展的决定因素。尿蛋白加重肾损伤的机制包括:①尿蛋白对肾小球系膜细胞和足细胞的毒性作用:大分子蛋白在系膜细胞中穿行可激活一系列信号通路,使系膜细胞增生并分泌细胞外基质(ECM)成分,导致肾小球硬化;②尿蛋白对近端肾小管上皮细胞的直接毒性作用:大量蛋白质进入肾小管腔超过肾小管重吸收能力时,可引起肾小管结构和功能的改变;③尿白蛋白通过损伤的肾小球内皮细胞发生渗漏,与肾小管上皮细胞接触可以改变其生物活性和生长特性,影响细胞因子及基质蛋白的表达,出现细胞转分化、凋亡等,导致肾小管-间质损害,肾功能持续减退。
(六)脂质代谢紊乱
高脂血症是慢性肾脏疾病的重要特征和独立的危险因素之一。高脂血症引起肾损伤的主要机制是:①脂蛋白沉积于肾小球系膜区,刺激系膜细胞增殖和细胞外基质产生,导致肾小球硬化;②血脂异常,尤其是氧化型低密度脂蛋白增加导致血管活性介质(包括内皮素-1、一氧化氮和血管紧张素Ⅱ等)及炎症因子大量释放,不仅在动脉粥样硬化的致病过程中起着重要作用,而且通过损伤内皮细胞导致肾脏损伤;③增加肾小球基底膜通透性,并通过产生具有细胞毒性的过氧化亚硝酸盐而导致肾脏细胞凋亡;④过量的游离脂肪酸可通过多种机制损伤足细胞、近端肾小管上皮细胞和间质组织,加重肾小球和肾小管病变。
(七)尿毒症毒素
1.小分子物质
分子量<500,包括无机物质中的无机磷、氢离子、某些酸根(如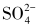 )和有机物质中的尿素、肌酐、尿酸、胍类、酚类和胺类等。尿素的神经毒性与其代谢产生的氰酸盐有关,后者可干扰高级神经中枢的整合功能。肌酐达到一定浓度时能引起细胞寿命缩短、溶血,还可以引起嗜睡、乏力等神经肌肉系统的功能异常。胍类毒素在积聚到一定量时,可引起多系统损害。
)和有机物质中的尿素、肌酐、尿酸、胍类、酚类和胺类等。尿素的神经毒性与其代谢产生的氰酸盐有关,后者可干扰高级神经中枢的整合功能。肌酐达到一定浓度时能引起细胞寿命缩短、溶血,还可以引起嗜睡、乏力等神经肌肉系统的功能异常。胍类毒素在积聚到一定量时,可引起多系统损害。
2.中分子物质
分子量为500~5 000,主要是一些多肽类物质,可引起周围神经病变、尿毒症脑病、糖耐量异常,还对细胞生成、白细胞吞噬、淋巴细胞与纤维细胞增生有明显的抑制作用。
3.大分子物质
分子量>5 000。目前认为这些物质主要是一些内分泌激素,如生长激素、甲状旁腺激素(parathyroid hormone,PTH)、促肾上腺皮质激素、胰高血糖素、胃泌素及胰岛素等,其中以PTH和胰岛素的细胞毒性作用最为突出。此外,β2微球蛋白引起全身性淀粉样病变已为人们所熟知。
(八)细胞介质、血管活性因子、生长因子等
1.促炎症分子
通过激活补体,亦或刺激局部淋巴细胞、单核/巨噬细胞和血小板聚集而导致局部炎症反应。
2.炎症小体
炎症小体(inflammasome)是在胞质内组装而成的多蛋白复合物,是宿主先天防御免疫系统的关键组成部分。几种类型的炎症小体,如NLRP3、NLRP1、NLRC4和AIM2已被确定,其中NLRP3是CKD的重要致病机制,也是潜在的治疗新靶点。
3.血管活性物质
血管紧张素Ⅱ(AngⅡ)作为缩血管物质主要是优先收缩肾小球出球小动脉,增加肾小球跨毛细血管压而损害肾小球,促进肾小球硬化。此外,AngⅡ和醛固酮还可以激活转化生长因子-β/Smad途径、1型纤溶酶原激活物抑制剂及其他细胞因子,加重肾小球、肾脏间质的损伤,该作用不依赖于其血流动力学效应。
4.生长因子
主要介导肾组织损伤以后的过度修复,如转化生长因子 β(transforming growth factor-β,TGF-β)、血小板衍生生长因子(platelet derived growth factor,PDGF)和胰岛素样生长因子1(insulin-like growth factor,IGF-1)等均能直接刺激肾小球系膜细胞增生,分泌ECM等。
5.ECM与蛋白酶
正常情况下肾组织中蛋白和ECM处在一个合成和降解的动态平衡状态下,在肾小球和肾小管-间质纤维化过程中,这种平衡往往被打破,即蛋白合成增加、各种蛋白酶活性下降、ECM合成增多而降解不足。
(九)免疫系统改变
免疫系统包括直接免疫和间接免疫作用,直接免疫介导的肾脏疾病通常是针对肾脏抗原产生自身抗体的结果,如抗肾小球基底膜病中的Ⅳ型胶原。体内免疫失衡会引起免疫细胞的持续性募集和肾脏损伤的加重,肾脏组织修复的不协调可导致肾脏重要结构发生纤维化,引起肾功能减退。许多肾脏疾病还与年龄密切相关。
(十)遗传学背景
在过去的数十年中,CKD相关基因以及基因变异的检测方法有了长足的进步,主要的突破包括:载脂蛋白L1(apolipoprotein L1,APOL1)与非糖尿病肾病的关联、糖尿病肾病相关基因和常染色体显性遗传的肾间质病变等。
2001年,美国肾脏病基金会-肾脏病预后质量倡议(National Kidney Foundation Kidney Disease Outcomes Quality Initiative,NKF-KDOQI)首次提出“CKD”概念,并在2002年发布了关于CKD定义、分期、评估的指南,这对于CKD的诊疗和管理产生了深远的影响。NKF-KDOQI指南里具体定义为:①肾脏损伤(肾脏结构或功能异常)≥3个月,可以有或无肾小球滤过率(GFR)下降,临床上表现为病理学检查异常或肾损伤(包括血、尿成分异常或影像学检查异常);②GFR<60ml/(min•1.73m2)≥3个月,有或无肾脏损伤证据。同时,根据肾小球滤过率(glomerular filtration rate,GFR)水平,将 CKD 分为 1~5期。
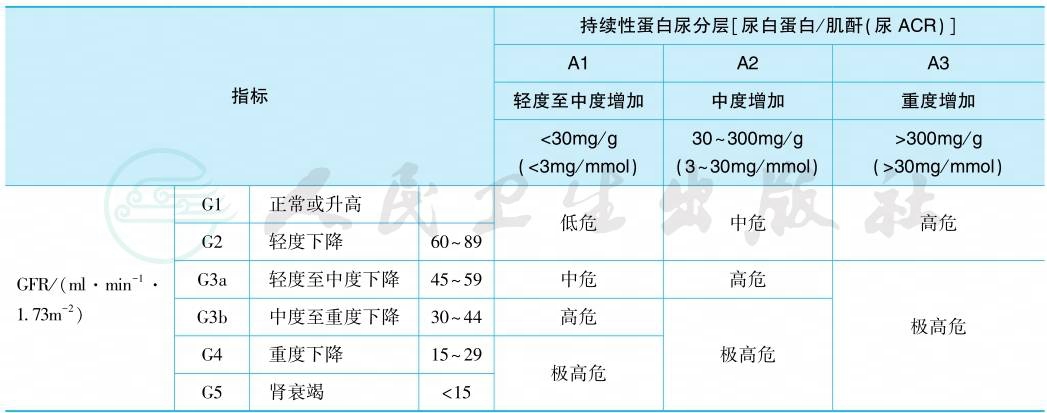
2009年和2012年,改善全球肾脏病预后组织(Kidney Disease:Improving Global Outcomes,KDIGO)对 CKD 的定义和分期作了进一步修改,将尿蛋白含量作为判断预后的新增指标,并将CKD3期细分为 CKD3a[GFR 45~59ml/(min•1.73m2)]和CKD3b[GFR 30~44ml/(min•1.73m2)]两个阶段(表1)。
表1 2012年KDIGO指南中CKD分期