英文名称 :lupus nephritis
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种病因未明的多系统累及自身免疫疾病,人群发病率为(30~50)/10万。我国约50%初发SLE患者就伴有肾脏累及,即狼疮性肾炎(lupus nephritis,LN)。LN是我国最常见的继发性肾小球肾炎,是SLE发病和死亡的主要原因。
SLE的病因仍不清楚,但明显涉及多种因素,其中包括遗传、激素、免疫和环境因素等具有研究证明。
免疫调节异常是SLE的主要问题,失去对细胞核自身抗原的免疫耐受是SLE的中心机制。CD8+效应性T淋巴细胞杀伤靶细胞,释放出核小体等自身抗原。树突细胞呈递自身抗原给T淋巴细胞。树突细胞表面的T淋巴细胞受体的异常可增加自身抗原的免疫原性。含DNA与RNA的自身抗原分别通过TLR9、TLR7激活树突细胞。抗原提呈细胞以自身抗原为第一信号,以共刺激分子如B7/CD28/CTLA-4为第二信号,活化T辅淋巴细胞。正常情况下,调节性T细胞可以抑制这个过程。但SLE患者CD4+CD25+调节性T细胞减少。而且,SLE患者2型T辅助淋巴细胞因子过度产生,导致B淋巴细胞持续活化、向浆细胞分化增多,自身抗体持续产生。
不同的临床表现是自身抗体形成及免疫复合物(immune complex,IC)产生的直接或间接结果。临床患者自身抗体包括抗核抗体(antinuclear antibody,ANA),其中高滴度的抗双链DNA(anti-double strand DNA,dsDNA)抗体、抗 Sm 抗体对诊断SLE有高特异性。自身抗体可以和肾小球抗原结合,引起免疫炎症。自身抗体也可以同肾小球上已种植的自身抗原结合,或形成自身抗原抗体复合物经循环沉积于肾小球内。在肾脏的IC可以固定补体,引起免疫炎症。此外,IC还能激活其他炎症反应,上调及激活内皮细胞上的黏附分子,从而募集白细胞及启动自身免疫损伤。被激活及损伤的肾小球细胞、浸润的巨噬细胞及细胞产生的炎性因子,使肾脏损害进一步扩大。
(一)肾小球病变
LN肾脏的组织病理变化多样,不同患者、不同肾小球,甚至在不同时间肾脏病理也会发生变化,既可是自发的改变,亦可与治疗相关。
肾小球内细胞增生及浸润是本病的基本病变,致肾小球呈分叶状,部分细胞出现核碎裂。肾小球内免疫复合物沉着是本病的第二基本病变,可沉积于上皮下、内皮下、基底膜及系膜区。免疫荧光可见 IgG、IgM、IgA、补体 C3、C1q阳性,常称为“满堂亮”表现。
2003年国际肾脏病学会/肾脏病理学会(International Society of Nephrology/Renal Pathology Society,ISN/RPS)LN 分型是目前公认的病理分类标准。分型如表1所示。
由于ISN/RPS分型标准主要依赖光镜,2018年国际肾脏病理工作小组对LN病理类型和肾组织活动性指数(activity index,AI)和慢性指数(chronic index,CI)评分标准提出建议,对Ⅳ型LN不再区分球性和节段性,同时建议所有类型使用AI/CI评分系统。
表1 2003年ISN/RPS狼疮性肾炎病理分型
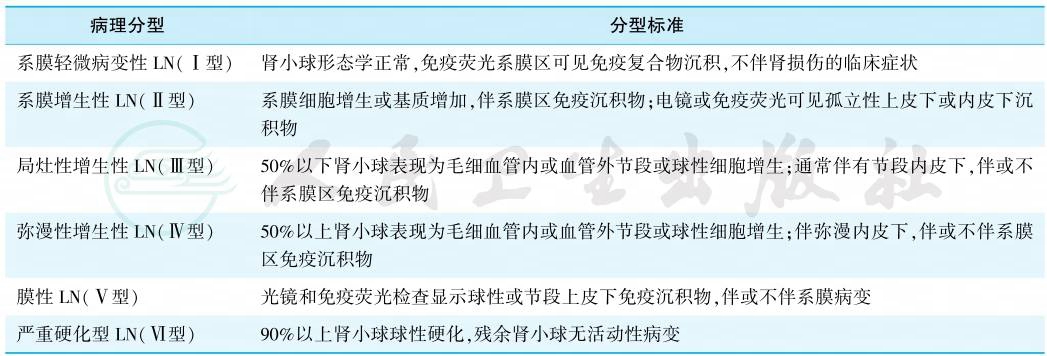
注:Ⅲ型或Ⅳ型LN如果光镜、免疫荧光或电镜提示肾小球上皮侧有广泛(>50%血管袢)免疫沉积物,通常提示同时存在Ⅲ+Ⅴ型,或Ⅳ+Ⅴ型。
(二)间质、血管病变
1.小管间质性肾炎
小管间质性肾炎(间质浸润、小管损害)伴或不伴小管基底膜IC沉积十分常见,常与其他肾小球病变同时存在。小管间质受累程度是判断预后的一个重要指标,它同高血压、血肌酐水平及临床病程进行性发展呈正相关。
2.血管病变
LN常见的肾血管受累,对肾脏预后造成不良影响。包括恶性小动脉性肾硬化、免疫复合物沉积、非炎症性坏死性血管病变、坏死性血管炎和血栓性微血管病。肾小球血栓性微血管病和LN并存时容易漏诊,需要光镜结合电镜加以鉴别。
3.肾小球足细胞病
SLE通过非免疫复合物沉积途径介导,多归入Ⅱ型LN。临床表现为肾病综合征,组织学特征为弥漫性足突融合,系膜区无或少量IC沉积,无内皮下或上皮侧电子致密物沉积。











