中文别名 :抗中性粒细胞胞浆抗体相关性小血管炎
系统性血管炎(systemic vasculitis,SV)是一组以血管壁的炎症和纤维样坏死为病理特征,以多器官系统受累为主要临床表现的疾病。一般来说,特定的血管病变同受累血管的大小、类型及分布相关联。肾脏血管分布丰富,因此它是SV中最常见的受累器官。临床上按病因又常将血管炎分为原发性和继发性,其中原发性(占70%)病因不明,继发性(占30%)是指继发于其他疾病如感染、系统性红斑狼疮、类风湿关节炎、过敏性紫癜及混合性冷球蛋白血症等。本文主要讨论原发性系统性血管炎。
为统一血管炎的分类标准,1994年在美国的Chapel Hill召开了有关系统性血管炎命名的国际会议。会议根据受累血管的大小将系统性血管炎分为三类即大血管炎、中等血管炎和小血管炎(表1)。
表1 Chapel Hill系统性血管炎命名国际会议所采取的血管炎名称和定义
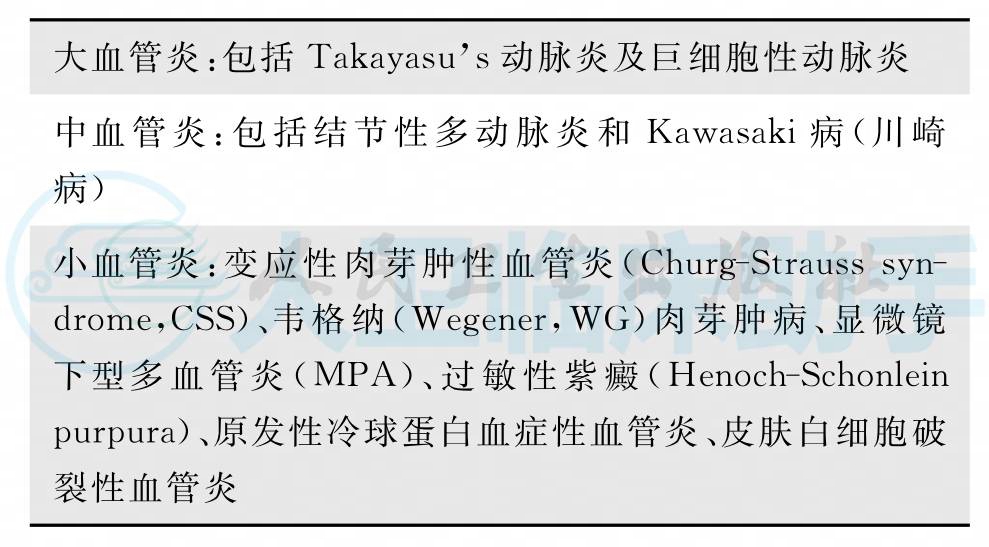
在2011年1月,美国风湿病学院董事局、美国肾脏病协会及欧洲抗风湿病联盟推荐将韦格纳肉芽肿病改命名为肉芽肿伴结节性多动脉炎,简称GPA,随着这一新名字被广泛认知,韦格纳肉芽肿病这一命名将逐渐被替代。
抗中性粒细胞胞浆抗体(anti-neutrophil cytoplasmic antibodies,ANCA)是一种以中性粒细胞和单核细胞胞浆成分为靶抗原的自身抗体,已经成为部分原发性小血管炎的特异性血清学诊断工具。目前将WG、MPA、CSS和寡免疫复合物型节段坏死性新月体性肾炎(NCGN)统称为ANCA相关性小血管炎(ANCA-associated systemic vasculitis,AASV),为本文讨论重点。
ANCA是一类对中性粒细胞嗜天青颗粒(一级颗粒)和(或)二级颗粒及单核细胞溶酶体成分的抗体。应用间接免疫荧光技术观察酒精固定的中性粒细胞,可发现ANCA有两种分布形式:抗体在胞浆呈均匀分布,称C-ANCA,这些抗体通常直接对抗丝氨酸蛋白酶(PR3),在WG中多见。另一种呈环核分布称P-ANCA,通常直接对抗髓过氧化酶(MPO),多见于MPA及特发性坏死性肾炎。两者同时存在,多见于肾及肺小血管炎同时存在的患者中。ANCA可能通过以下机制发挥作用:
1.ANCA和中性粒细胞的相互作用
ANCA可以在体外进一步激活预先处理过的中性粒细胞,导致中性粒细胞发生脱颗粒反应,产生大量具有致病性的氧自由基和释放中性粒细胞颗粒中的各种蛋白酶。人体实验研究显示,在ANCA阳性的血管炎患者的肾穿刺标本中,被激活的中性粒细胞数目增多,并与疾病的严重程度成正比。在这些患者中,循环中性粒细胞产生的反应性氧自由基亦增加。中性粒细胞的功能可因静脉甲泼尼龙脉冲而恢复正常,可能与一种抗氧化酶———过氧歧化酶的基因逆向调节有关。
ANCA的致病作用同中性粒细胞的激活状态密切相关。ANCA对静止的中性粒细胞作用有限,这是因为PR3 和MPO位于胞浆,相对来讲不容易同抗体结合,但当中性粒细胞在体外预先同肿瘤坏死因子(TNF)一起培育后,ANCA对中性粒细胞的激活程度将增强,因为TNF增强了抗原性物质如MPO在细胞表面的表达。此外,TNF及其他细胞因子(如IL-6)本身也能直接引起肾脏损伤。
另外,当患者有循环ANCA存在时,感冒及炎症所致中性粒细胞释放的MPO对局部的炎症过程起促进作用。在WG患者中,感冒样症状或感染可使病情恶化即是证明,这可以解释在部分WG患者中磺胺增效剂(TMPSMZ)在感染早期应用可使病情得到缓解,但亦有持相反意见者。
2.中性粒细胞、ANCA和内皮细胞的相互作用
ANCA介导的中性粒细胞脱颗粒反应,使内皮细胞直接暴露于蛋白酶的损伤之下。此外,ANCA可以激活内皮细胞,包括使内皮细胞通透性增高,使内皮细胞表面更容易黏附炎症细胞和血小板,并导致内皮分泌细胞因子增多。体外研究发现抗MPO抗体和抗PR3抗体可以刺激中性粒细胞并损伤内皮细胞。进一步的研究发现内皮细胞与PR3、 MPO的结合可以造成血管损伤,但其机制尚不清楚。
对于内皮细胞是否产生及经激活而表达PR3有不同意见。在ANCA相关性血管炎中,先有内皮细胞活跃,使炎性细胞在血管受损部位的吸附增强,随之释放的PR3及其他中性粒细胞蛋白酶可诱导内皮细胞合成及分泌白细胞介素(IL-8),一种中性粒细胞化学吸附剂,由此吸引更多的中性粒细胞。中性粒细胞及内皮细胞所释放的PR3及其蛋白酶经吸附分子ELAM及VCAM-1的诱导,可增强中性粒细胞及单核细胞在内皮细胞表面的吸附。可溶性内皮细胞蛋白C受体提高PR3与激活的中性粒细胞相结合,为中性粒细胞引发血管炎症———凝血瀑布样病变提供了链接,这也许能部分地用于解释为何WG患者中静脉血栓发生的危险性增加。在AASV的发病机制中,内皮细胞究竟是积极参与还是仅为旁观者尚不清楚。但带正电荷的蛋白酶和趋化性肽的持续释放以及ANCA与内皮细胞的结合,都将对初始反应进行放大,从而导致炎症的进展和持续的血管损伤。
3.ANCA激活单核细胞
AASV患者的肾脏病理标本可见单核细胞和巨噬细胞,他们通过合成和分泌一系列趋化因子、生长因子和细胞因子参与肉芽肿的形成。由于一些ANCA的靶抗原是单核细胞的成分,因此这些单核细胞通常可以成为ANCA攻击的靶目标,并可以被ANCA所激活。有体外实验证实ANCA可以刺激单核细胞产生MCP-1,其通过促进局部单核细胞的聚集而参与肉芽肿的形成。
4.ANCA与抗内皮细胞抗体(anti-endothelial cell antibodies,AECA)的相互作用
抗内皮细胞抗体是一组针对内皮细胞相关抗原的自身抗体的总称。它可与一些细胞因子及炎症因子互为因果,共同参与内皮细胞的损伤过程。有研究表明:AECA、ANCA及各种黏附因子、炎症因子与内皮细胞、中性粒细胞互相影响,从而引起周而复始的免疫反应,造成持续的血管壁或组织损伤。
5.T细胞在AASV致病中的作用
有许多证据提示T细胞可能参与了AAVS的发病机制。血管炎性病变或肉芽肿中存在许多T细胞,在AASV中T细胞被激活并有抗原驱动的T细胞增生反应;GPA患者活动期血CD4水平及单核细胞活性较缓解期及正常对照者显著升高;对于难治性血管炎的患者,可以通过针对T细胞的治疗使病情得到缓解等。
原发性小血管炎具有非免疫复合物性小血管炎的基本病理特征。免疫病理无或仅有少量免疫球蛋白或补体成分在病变处沉积,故又称寡免疫复合物沉积性小血管炎,肾脏是AAVS最易受累的器官,无论MPA、WG或CSS其肾脏病理变化基本相同,即以寡免疫复合物沉积性新月体肾炎为特征。光镜下,绝大多数患者表现为局灶节段性肾小球毛细血管袢坏死和新月体形成。与免疫复合物介导的新月体肾炎不同,一般肾小球内无明显细胞增生。肾小球毛细血管袢坏死区域肾小球基底膜断裂,鲍曼囊壁粘连、破裂,肾小球周围可伴有多核细胞。结节性多动脉炎以中等大小动脉累及为特征,而小血管(包括小动脉、小静脉和毛细血管)的累及通常为WG及MPA的特征。近年来,肾小管病变及间质单核细胞浸润及纤维化也受到重视。晚期则表现为肾小球硬化、间质纤维化及肾小管萎缩。免疫荧光通常没有或寡免疫复合物沉积,电镜下也未观察到免疫复合物性电子致密物的沉积。然而近年来随着对AASV认识的深入,发现肾脏病理有免疫复合物沉积者不断增多。











