英文名称 :intracranial tumors
颅脑与脊髓肿瘤既可以来源于颅脑和椎管内的结构,也可以来源于它们之外的结构,前者称为原发性,后者为继发性。原发性脑脊髓肿瘤的年发病率颅内肿瘤为(4~10)/10万,脊髓肿瘤为(0.9~2.5)/10万。近年来,随着诊断技术的提高和人均寿命延长,脑脊髓肿瘤的发病率有上升趋势。
至今脑脊髓肿瘤发病原因未完全明确,有下列几种可能病因。
(一)遗传因素
虽然绝大多数脑瘤散发发病,但是大量研究显示,1%~5%的脑瘤有多种遗传性因素并具有家族性,如斑痣性错构瘤(phakomatosis)。常见的有:①神经纤维瘤病(NF):Ⅰ型为多发性神经纤维瘤病,又称von Recklinghausen病;Ⅱ型为具有双侧听神经瘤和/或其他神经系肿瘤。两型均可有先天畸形(如大头畸形、脊柱侧弯畸形、蝶骨小翼和眶板缺失等),或中枢神经系统其他肿瘤,如脑膜瘤、毛细胞型星形细胞瘤等。②胶质瘤:多数没有遗传性,少数有。如神经纤维瘤病Ⅱ型、结节性硬化、Gardner综合征、Turcot综合征及Li-Fraumeni综合征。③血管网状细胞瘤:约1/5血管网状细胞瘤伴有全身其他脏器的血管性肿瘤,如视网膜血管网状细胞瘤、肾脏或胰腺的血管瘤等。此类血管网状细胞瘤又称为von Hippel-Lindau病(VHL),具有家族史。
(二)生物因素——病毒
已发现腺病毒、乳多泡病毒、猴空泡病毒、肉毒病毒、Oncorna病毒等可诱发脑瘤,但主要见于动物。目前尚未获得病毒引起人脑肿瘤的直接证据。
(三)物理因素
1.放射线
1974年Modan随访了11 000名因头癣接受放射治疗的儿童,脑膜瘤的发病率较对照组自然情况下增加4倍,且多数伴有放疗后头皮改变及脱发。此后有作者指出放疗后脑膜瘤的发生时间与放射剂量相关,放射剂量越高,发生时间越短。放疗也可引起胶质瘤、海绵状血管瘤等。
2.外伤
文献报道在头颅外伤的局部骨折或瘢痕处出现脑膜瘤的生长,甚至在脑膜瘤中找出铁丝,认为局部异物或瘢痕对正常脑膜或脑组织长期刺激可导致肿瘤的生长。流行病学调查头颅外伤患者中,脑瘤的发生率并未有明显提高。因此,损伤对中枢神经系统的致瘤性有待进一步明确。
(四)化学因素
多种化学物品可诱发动物脑瘤,如甲基胆蒽、多环烃类(PCH)与烷化剂等,氯代乙烯是目前认为最可能引起人脑肿瘤的化学制剂。从8个流行病学研究调查来看,从事氯代乙烯生产的工人脑瘤发病率要稍高。
(五)先天因素
在胚胎发育过程中有些细胞或组织可停止发育分化而遗留于神经系统内。这些残留的组织尚有分化的潜能,并可发展成为肿瘤。常见的先天性肿瘤有颅咽管瘤、脊索瘤、上皮样及皮样囊肿、畸胎瘤等。
早期脑、脊髓肿瘤的分类较混乱,Virshow(1821~1902)提出了胶质瘤的概念。Cohnheim与Ribbert提出脑肿瘤与胚胎残留有关,Bailey与Cushing(1926)和Kernohan(1949)分别对中枢神经系统肿瘤和神经外胚叶肿瘤进行了分类。1978年以来,WHO在多国专家合作基础上,先后发表了多个版本的中枢神经系统肿瘤分类。以下为2007年WHO对中枢神经系统肿瘤的分类(表1)。
表1 2007年WHO对神经系统肿瘤的分类与分级

续表

续表

续表

续表

1.ICD-O为国际疾病(肿瘤)分类(International Classification of Diseases for Oncology)的简称。分子代表肿瘤编号,分母/0代表良性肿瘤,/1代表低度或不肯定恶性或临界恶性,/2为原位恶性肿瘤,/3为恶性肿瘤。
2.WHO(世界卫生组织)Ⅰ级代表良性,Ⅱ级代表低度或临界恶性,Ⅲ级代表恶性,Ⅳ级代表高度恶性。
3.在1993年WHO神经系统分类中有垂体瘤,但在2000年分类中却删去。
颅内肿瘤可生长于脑外、脑内、脑室内或在蛛网膜下腔等。肿瘤本身和瘤周水肿等常推移、压迫或破坏脑组织。因此,肿瘤所产生的临床症状取决于肿瘤的部位、肿瘤的生长方式及肿瘤的生长速度。由于脑组织、脑血管及脑脊液在一定时间内可通过代偿机制维持正常的颅内压,因此相同体积的肿瘤生长迅速快的较生长缓慢的更易出现颅高压症状。一般肿瘤生长速度受到下列因素影响:①出血,见血供丰富的肿瘤;②坏死,因瘤细胞生长过快,血供不应求所致;③囊变,常继发于坏死、出血;④间变,由低级别肿瘤向高级别演变。良性肿瘤多有包膜,呈膨胀性生长;恶性者呈浸润型生长,无包膜。脑瘤复发大多数在原位,也可发生颅内转移。
过去认为脑组织是免疫特免器官,现经研究证明大部分脑有免疫功能。脑内不仅有功能类似巨噬细胞的小胶质细胞,而且有T淋巴细胞,特别是病变时,后者可经血-脑屏障入脑。这不仅解释中枢神经系统自身免疫病(如多发硬化),而且为脑瘤的免疫治疗提供了科学依据。但是,迄今脑胶质瘤的免疫治疗不理想,其中重要原因之一是脑肿瘤细胞的免疫逃逸机制:①肿瘤微环境诱导T细胞功能障碍,这与B7家族负性共刺激分子有关;②瘤细胞分泌细胞因子如TGF-β、IL-10等,抑制机体的免疫反应;③瘤细胞下调其表面组织相容性复合体(MHC)等分子的表达,从而削弱其免疫原性。因此,寻找脑瘤的特异性抗原,攻克肿瘤的免疫逃逸是脑瘤免疫治疗的方向。
原发脑瘤的发生发展是一个多步骤过程,涉及抑癌基因的失活和原癌基因的激活和过度表达,也有细胞周期调节的变化、信号通路的异常等。目前,根据肿瘤基因表达的情况将原发性多形性胶母细胞瘤(GBM)分为四个亚型:①经典型(classical):具有高增殖活性的特征,此型对放疗反应好;②间叶型(mesenchymal):与间叶组织及血管生成有关,此型对强放化疗有效,并可能对抑制Ras、P13κ或者抗血管生成的药物反应好;③神经型(neural):基因表达与正常神经组织的特征性基因表达很相似,肿瘤对周围组织侵袭性较低;④前神经型(proneural):基因激活似神经元的分化过程,该型患者年纪轻,以血小板源性生长因子受体α(PDGFR-α)和IDH1/IDH2突变为特征,与继发GBM有类似的基因表达,提示继发GBM可能属此亚型。该型对HIF、P13κ或PDGFR-α等抑制剂药物有很好的反应。虽然对强放化疗几乎无反应,但预后好于其他三型(图1)。
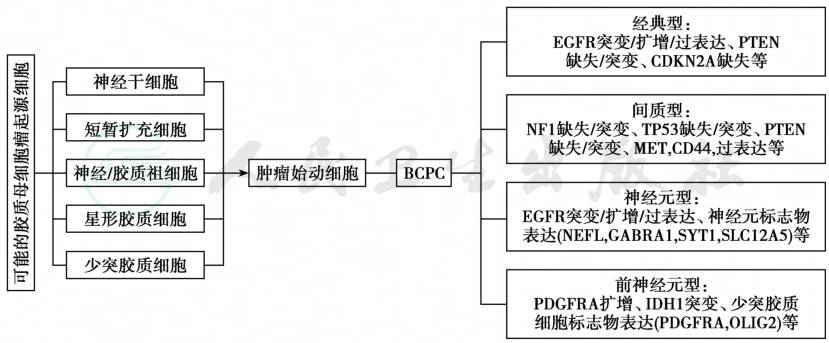
图1 胶母细胞瘤的亚型分类
目前,对原发性与继发性的多形性胶母细胞瘤在分子水平改变的区别已取得了较为一致的看法。原发性多形性胶母细胞瘤分子生物学改变以EGFR的扩增与过量表达为主,而继发性胶母细胞瘤则以P53的突变为主要表现。原发性胶母细胞瘤中P16的突变发生率是继发性的2倍。在较少见的巨细胞胶母细胞瘤中75%以上有P53的突变,而EGFR、CDK4的扩增及P16的丢失或突变极少发生,因此有作者认为此类胶质瘤在发生上与继发性胶母细胞瘤相似。
除了星形细胞胶质瘤之外,在其他中枢神经系统肿瘤中亦有基因异常改变的发现。研究发现在少突胶质瘤中有1p和19q等位基因的丢失,而在儿童室管膜瘤中有位于6q上的基因片段的丢失。以往研究表明,在约50%的髓母细胞瘤中存在17p13的丢失。然而最近认为,p53并非髓母细胞瘤的特异性基因改变,目前已更为精确的定位于17p13.2-13.3,这一区域并不包括p53基因,而在这一区域中的HIC-1与OVCA1基因的丢失可能与髓母细胞瘤的发生有着密切的关系。
近来发现在胶质母细胞瘤和髓母细胞瘤中,存在很少量具有自我更新和多向分化能力的细胞,它们有神经干细胞一样的标志物,且对目前各种治疗方法如放疗、化疗、免疫治疗等均不敏感或具有抵抗或逃逸能力。这种细胞的发现无疑为脑瘤的发生发展、治疗和复发防治提供了新方向。











