中华医学会耳鼻咽喉科学分会及中华耳鼻咽喉科杂志编委会于2002年对阻塞性睡眠呼吸暂停低通气综合征(obstructive sleep apnea hypopnea syndrome,OSAHS)给出的定义是指睡眠时上气道塌陷阻塞引起的呼吸暂停和通气不足、伴有打鼾、睡眠结构紊乱,频繁发生血氧饱和度下降、白天嗜睡等病征。呼吸暂停是指睡眠过程中口鼻气流停止≥10s。低通气(通气不足)是指睡眠过程中呼吸气流强度较基础水平降低50%以上,并伴动脉血氧饱和度(arterial oxygen saturation,SaO2)下降≥4%。睡眠呼吸暂停低通气(通气不足)指数(apnea hypopnea index,AHI)是指平均每小时睡眠中呼吸暂停和低通气的次数(单位:次/h)。阻塞性呼吸暂停是指呼吸暂停时口鼻无气流通过,而胸腹呼吸运动存在。
Wodd早在1810年就注意到过度肥胖的患者并发周期性呼吸和白天嗜睡。1918年,Olser描述了一种肥胖、嗜睡、发绀综合征,因其与英国作家狄更斯在其名著《匹克威克外传》中所描述的主人公Joe的形象相似,故称其为皮克威克综合征(Pickwickian syndrome)。Kerr等又发现这些患者有心脏——循环系统的异常。Burwell(1956)报道此征的表现为肥胖、嗜睡、肺泡换气不足和肺源性心脏病。Gastaut(1965,1966)相继论及间歇性气道阻塞可引起嗜睡与肺动脉高血压症,所谓这种患者在睡眠时可出现多次发作性呼吸暂停。此后,有关报道增多,对此征的阐述更为明确。
鼾声(snore)是睡眠期间上呼吸道气流通过时冲击咽黏膜边缘和黏膜表面分泌物引起振动而产生的声音;其部位始自鼻咽,直至会厌(图1),包括软腭、悬雍垂、扁桃体及其腭咽弓和腭舌弓、舌根、咽肌及咽黏膜。响度在60dB以下的鼾声,往往属于正常现象;若鼾声响度超过60dB以上,妨碍上呼吸道呼吸气流的通过,影响同室人休息或导致他人烦恼时则称鼾症(snoring disease)。鼾症较轻者(单纯型)不引起明显的缺氧症状;重者(憋气型)鼾声响度可达80dB以上,并可伴有不同程度的缺氧症状,此种鼾症实为阻塞性睡眠呼吸暂停综合征的同义词了,因为鼾声乃系阻塞性睡眠呼吸暂停综合征的一个十分突出的症状。
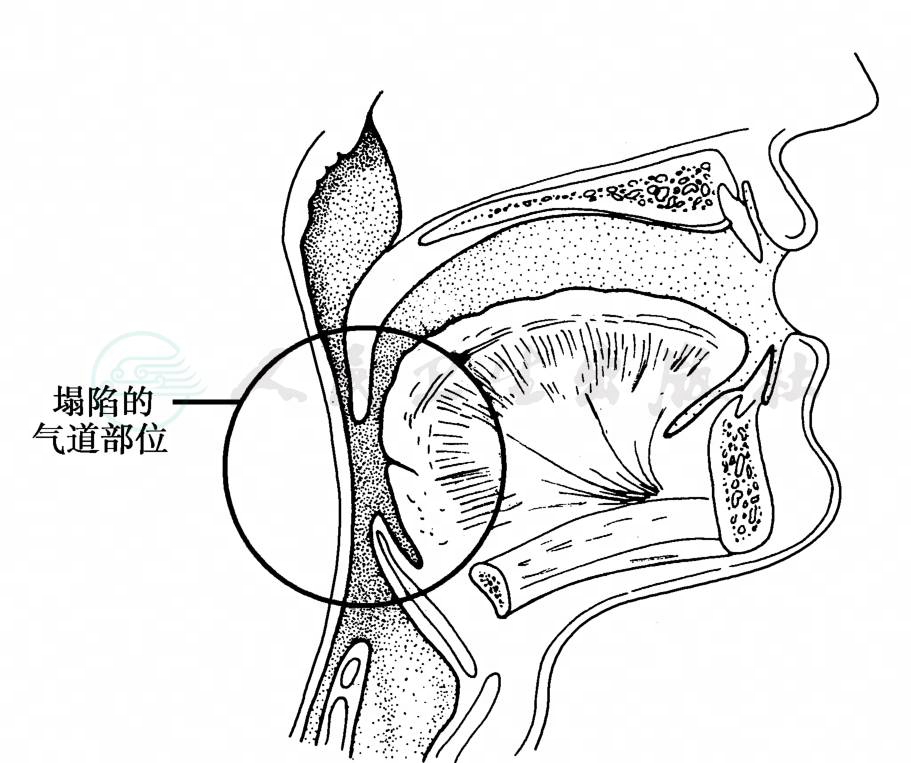
图1 鼾声发生的部位
注:鼾声发生于自会厌到鼻咽的没有坚硬支架的气道塌陷部位 (包括软腭、悬雍垂、扁桃体、腭弓、舌根、咽部肌肉与黏膜)。
肥胖者脂肪蓄积过剩,增加呼吸和循环系统负担,入睡后肌张力低下,因而咽腔缩小,更易发出鼾声。
近些年来,一些神经科、呼吸科、小儿科、耳鼻咽喉科医师和临床睡眠学家都对睡眠与呼吸之间的关系产生了巨大的兴趣,就睡眠呼吸暂停综合征做了不少的深入观察和研究工作。
中枢型的病因已在分型中述及。上呼吸道任何解剖部位的狭窄或堵塞,都可导致阻塞性睡眠呼吸暂停。
(一)鼻腔及咽、喉部病变
前鼻孔狭窄或闭锁,鼻中隔偏曲,鼻息肉,肥厚性鼻炎,变应性鼻炎,鼻腔各种良性或恶性肿瘤;鼻咽炎,腺样体肥大,鼻咽部闭锁或狭窄,扁桃体肥大,悬雍垂过长或肥大,咽部肿瘤,咽肌麻痹;会厌炎,会厌囊肿,会厌肿瘤,声门上水肿,声带麻痹,喉蹼,喉软骨软化;以及颈部的甲状腺肿和其他原发性或转移性肿块压迫等。
(二)口腔病变
以舌的病变影响为甚,如巨舌症,舌肿瘤,舌根部异位甲状腺,继发于黏液性水肿的舌体增大,用咽瓣修复腭裂的部分患者。
(三)某些先天性颌面部发育畸形
如①皮埃尔-罗班综合征(Pierre-Robin syndrome),其特征为小颌、腭裂、硬腭高拱、舌下垂等;②普拉德-威利综合征(Prader-Willi syndrome),主要表现为吞咽困难,肥胖,面部畸形,性功能低下,智力迟钝等;③唐氏综合征(Down syndrome),有鼻梁低平,上颌发育不全、下颌圆小、高腭弓、智力迟钝等特点;④特雷彻·柯林斯综合征 (Treacher Collins syndrome),表现为下颌与面骨发育不全,如下眼睑缺损、眶上缘畸形、小颌、颌面骨下陷、腭裂、会厌畸形及耳畸形等;⑤克鲁宗综合征(Crouzon syndrome),主要有颅面骨发育不全,鼻梁低宽,钩形鼻鼻孔,鼻腔狭小,鼻中隔偏曲,上颌下陷,上唇短缩,硬腭高拱,下颌骨大而突出等;⑥Hurler-Scheie综合征,其临床特征介于Hurler综合征与Scheie综合征之间,特点为颏后缩(小颌),症状有智力迟钝、侏儒症、多种骨发育不全、角膜混浊、耳聋等。
(四)全身性疾病
肢端肥大症引起舌体增大,甲状腺功能减退所致的黏液性水肿,慢性淋巴细胞性白血病性咽峡炎,女性绝经期后的内分泌紊乱以及肥胖症等,均易导致OSAHS。肥胖者易发生OSAHS的原因可能为:①此类患者舌体肥厚,且软腭、悬雍垂和咽壁有过多的脂肪沉积,易致气道阻塞;②咽腔开放程度与肺的体积变化有关,肥胖者能明显减少肺体积,从而产生肥胖性肺换气不足综合征;此征可能是腹腔脂肪的增多导致其容量增加,使横膈升高,又因脂肪沉积在膈肌和肋间肌,降低了呼吸动作的力度,故易引起本征。
Fairbanks(1987)认为造成打鼾或阻塞性睡眠呼吸暂停的主要原因有4点:①腭肌、舌肌及咽肌的张力不够,在呼吸周期的吸气期,不能保持气道的开放;②软腭、悬雍垂过长,呼吸时导致鼻咽气道狭窄,并发生振动;③咽腔有占位性病变,从而侵占了咽部气道;④鼻腔通气受限,在吸气期可使塌陷性的气道部分产生更大的负压。
Gastaut等(1965,1966)采用张力仪(胸腔呼吸运动记录仪)与热敏电阻器(热敏电阻呼吸仪)检测技术,将睡眠呼吸暂停分为3型
(一)中枢型(CSA)
中枢型亦称膈肌型,即呼吸气流与膈肌运动均出现暂停(图2)。测量记录时,置于鼻咽部与口颊部的热敏电阻器在最后的气流通过后即记录不到气流,与此同时置于胸腹部的张力仪也不能描记到膈肌与胸壁肌的运动。Guilleminaut(1972)甚至把一个顶端带有压力传感器的导管置于食管下端,也没有记录到膈的运动。或谓中枢型者缺乏奋力呼吸(respiratory effort)。此乃呼吸中枢对血液中二氧化碳分压变化的反射性刺激发生障碍,导致各呼吸肌暂时停止运动,因而出现呼吸暂停。为何在睡眠时诱发或加重,Devereux(1973)认为:可能是由于自主呼吸障碍而随意呼吸保存,出现呼吸运动分离现象。即患者虽有自主呼吸障碍,但在觉醒时可借随意呼吸机制而保存相当的呼吸功能;一旦入睡,呼吸的随意控制消失,便出现自主呼吸障碍。中枢型不伴有明显鼾声。呼吸中枢受损及某些颅脑疾病如颅脑损伤、脑炎、脑肿瘤、延髓型灰白质炎、脑干梗死或药物中毒等为中枢型的常见病因。
(二)阻塞型(OSA)
阻塞型亦称周围型,由于上呼吸道阻塞,胸壁肌和膈肌虽出现持续性运动,但鼻腔与口腔却无有效的气流通过(图2)。即呼吸暂停时,胸腹部的张力仪记录到持续的奋力呼吸动作,但没有气流通过鼻咽部和口颊部的热敏电阻器。
(三)混合型(MSA)
混合型在开始时为一短暂的中枢型呼吸暂停,紧接着膈肌运动恢复之后延续为阻塞型呼吸暂停(图2)。
3型中,以阻塞型者为多见。
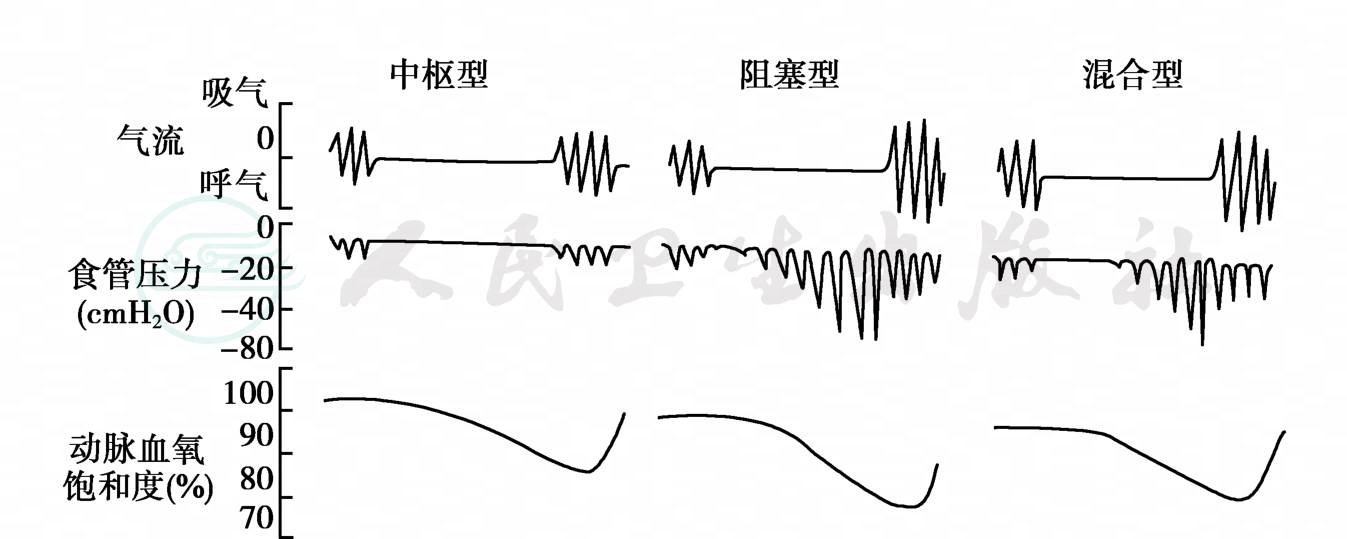
图2 睡眠呼吸暂停综合征三种类型的呼吸气流,奋力呼吸 (食管压力)和动脉血氧饱和度示意图
注:中枢型:缺乏呼吸气流和奋力呼吸;阻塞型:缺乏呼吸气流,但奋力呼吸继续存在;混合型:缺乏呼吸气流,起始亦无奋力呼吸,接着出现奋力呼吸 (即先出现中枢型,接着呈现阻塞型);动脉血氧饱和度:在所有三型中都相应下降。
本征的发病率尚难确定,目前可能低估了其实际的发病者数。Fairbanks(1987)估计美国的发病者数约有2~5百万人。据美国流行病学调查初步估计,40岁以上男性的患病率为1.24%。Fairbanks称,30~35岁的人群中,有20%男性和5%女性打鼾;60岁左右者,则有60%男性和40%女性打鼾;肥胖者打鼾的要比瘦者多3倍;严重的打鼾者与相同年龄和体重的不打鼾者相比较,前者患高血压症的可能性更多,且往往发展成为阻塞性睡眠呼吸暂停。Maniglia(1994)报告,睡眠呼吸暂停和打鼾是常见病征,美国成年男性的发生率约为5%~10%;打鼾则更为常见,约发生于50%男性和30%女性;鼾症可能是OSAHS的前驱阶段。
国内韩子刚等(1993)对13275人进行鼾症普查时发现,经常打鼾者占18.8%,属于鼾症者(含单纯型与憋气型)483例,占3.64%;其中憋气型鼾症(憋气是指每次呼吸暂停超过10秒,平均每小时睡眠发生憋气5次以上,普查时观察睡眠时间1小时以上)172例,占1.3%。鼾症发生率以45~59岁年龄组为最高,占8.23%,男性明显高于女性,超重型与肥胖型明显高于正常体型的人群。北京协和医院内科于1986~1987年期间对57例有睡眠呼吸障碍者进行多导仪监测结果,30例诊断为OSAHS,其中男占26例,女占4例,年龄为37~67岁,90%以上为大于40岁的患者。
总之,本征可发生于任何年龄,甚至婴儿和儿童,男女均可发病,但多见于40岁以上的男性;女性则多见于绝经期后,其病情多较男性为轻。少数患者可有家族史。
人们早已注意到睡眠时呼吸功能降低,表现为每分钟气流量减少。Sukerman等(1979)认为:在睡眠时,保持咽部气道的反射功能消失了,舌肌和咽腭肌等的张力降低,加之咽部气道在解剖上缺乏骨性支架,咽部的正常形状和气道的保持需要依赖感觉和肌肉的反射活动。在生理状态下,吸气时气道产生负压,气道扩张肌和咽肌等收缩,肌张力增大,维持气道开放。任何原因引起保持咽腔开放的肌肉张力减弱或咽腔负压增加,机体无力克服吸气时所出现的咽腔压力低于大气压的状态,就会使咽壁软组织被动性塌陷,出现上呼吸道的阻塞症状或呼吸暂停。持续较久的或反复的呼吸暂停,就会引起低氧血症和高碳酸血症,久之便导致全身诸多系统的病理生理变化。
(一)呼吸系统
由于睡眠时气道的气体交换受阻,出现呼吸暂停,导致动脉血氧分压下降,血二氧化碳分压上升〔>6.00kPa(45mmHg);正常为5.33kPa(40mmHg)〕,pH下降(<7.35;正常为7.35~7.45),引起呼吸性酸中毒,出现发绀、气促、躁动不安等症状,甚至发生呼吸骤停。
(二)心血管系统
正常人睡眠时肺动脉压和肺毛细血管压保持正常,体循环压较日间略低。呼吸暂停时,低氧可使交感神经兴奋,中心静脉血液回流增加,小动脉收缩,心输出量增多,引起肺循环和体循环压力上升,产生肺动脉甚至全身动脉压力周期性升高,从而可导致原发性高血压及肺源性心脏病。同时,低氧血症或高碳酸血症均可使肾上腺髓质中的儿茶酚胺释出增加,引起血压升高,心跳加快,甚至各种心律紊乱;如窦性心律失常,心搏徐缓,心动过速,心脏停搏等。在睡眠期间,若发生心脏停搏,即可导致突然死亡。心律失常是睡眠过程发生猝死的主要原因。
(三)血液系统
血氧过低可刺激肾脏、分泌红细胞生成素、循环血中红细胞增加,引起继发性红细胞增多症,导致血黏度增加,外周阻力增大,影响血流速度与循环功能。由于中枢神经系统的循环障碍,可出现一系列相关症状。
(四)神经系统
由于缺氧和循环障碍,神经系统特别是中枢神经系统可受到损害,出现头胀、头痛、头晕、耳鸣等症状。随着血氧饱和度下降,脑电图出现觉醒图形,表现为非快速眼动(NREM)睡眠与快速眼动(REM)睡眠减少或缺乏等睡眠结构紊乱,引起白天困倦、嗜睡;低氧引起的脑损害可造成智力减退、记忆力下降、性格改变或行为异常等。低氧血症时可使交感神经活性增强,CO2蓄积时则致副交感神经功能亢进。
(五)内分泌系统
垂体前叶(腺垂体)分泌的生长激素主要是在快速眼动睡眠期间释放出来的;患有阻塞性睡眠呼吸暂停的患儿,在睡眠期间生长激素的释放有不同程度的减少,这也是影响患儿生长发育的因素之一。
(一)病史询问和一般检查
向患者及其家属询问和了解夜间睡眠状况,有无大声打鼾及憋气现象,每次憋气大约多长时间和憋气发作的频度(以上情况还可嘱其家属进一步观察后再行提供),白天是否有嗜睡和精神、情绪的变化等。
有的患者肥胖(约占5%~39%),少数颈部粗短,下颌后缩、小颌或其他颌面畸形,有的并发高血压(约25%~40%);有的口咽较正常狭小,悬雍垂粗长,舌大而后置,扁桃体肥大等;有的可见到肥厚性鼻炎、鼻中隔偏曲、鼻息肉以及鼻和咽喉部其他病变或肢端肥大症等全身性症征。
(二)纤维鼻咽喉镜检查或电子鼻咽镜检查
可在清醒时和睡眠时分别进行检查。
1.清醒状态
将纤维鼻咽喉镜检查结合Müller动作进行,即纤维(或电子纤维)内镜检查上呼吸道时紧闭口、鼻,用力吸气(模拟近似憋气的状态),以观察口咽-软腭及喉咽-舌根平面等的关系。鼻腔与咽腔先行表面麻醉,取坐位和卧位各行纤维(电子纤维)鼻咽喉镜检查一次,以观察正常或异常情况。然后嘱患者在平静呼吸时和捏鼻闭口用力吸气时,分别观察软腭和舌根后移、咽侧壁向咽腔塌陷及会厌向喉内移动、缩小或遮盖喉入口的情况。若在做Muller动作时,咽壁软组织仅轻微向咽腔塌陷,即为轻度内陷;若咽壁软组织塌陷较明显,最狭窄部位的咽腔横截面积较做平静呼吸时缩小约1/2,即为中度内陷;若咽壁软组织塌陷更重,最狭窄部位的咽腔横截面积缩小约3/4,则为重度内陷;若咽壁塌陷部位的咽腔基本消失,在横截面上几乎不见腔隙,称为极度内陷。用此种检查方法和咽壁软组织塌陷的分级标准,可以判断阻塞性睡眠呼吸暂停时的阻塞部位及阻塞程度。检查过程中若有电视监护器显示则更有利于察看和判断。
2.睡眠状态
Abdullah等(香港中文大学医院,1994)曾为50名经多导睡眠描记法确诊为OSAHS患者和3名单纯打鼾者在用短效安定入睡后,用带有电视监护器的纤维鼻咽喉镜经局部麻醉的鼻腔,对上呼吸道进行动态变化的观察,可清楚看到打鼾时和睡眠呼吸暂停期间,口咽或喉咽的塌陷部位和程度,以及部分患者会厌软弱向喉内倾倒、遮盖喉入口,导致呼吸梗阻的情况。经此检查后,作者判定50名OSAHS患者中,根据其咽腔不同的阻塞部位,只有8人适合做悬雍垂腭咽成形术,术后效果满意。因此,电视睡眠可曲性鼻咽镜检查(video sleep flexible nasopharyngoscopy)有助于更好地选择手术适应证,从而提高手术的成功率。
(三)影像学检查
下列几种影像检查法可以根据具体情况选择应用
1.头测量法(cephalometry)
取坐位与卧位于吸气和呼气时分别对头部进行正、侧位X线拍片,然后测量后鼻棘至枕骨斜坡底,悬雍垂至咽后壁、会厌尖平面的舌根至咽后壁之间的距离。用此法检查可以发现有相当数量的OSAHS患者存在骨骼和软组织方面的畸形,借以判断上呼吸道阻塞的部位和程度,为制定手术方案和评价手术效果提供依据。De-Berry-Borowiecki等(1988)根据头测量法的结果认为OSAHS患者与正常人相比存在5个特点:①舌和软腭明显增大;②舌骨向下移位;③下颌骨的大小和位置可正常,但由于下颌体向下移位,使面部增长;④上颌骨位置偏后并且硬腭增长;⑤鼻咽部正常,但口咽和喉咽水平的气道平均缩小25%,因而引起或加重OSAHS。
2.透视电影(cinefluoroscopy)
快速连续CT扫描拍片或CT扫描电影、睡眠透视等,都是在患者清醒时或睡眠时对头颈部进行检查,从动态的或接近连续的影像上观察鼻咽部、咽峡部、舌体和舌后以及喉咽部气道的狭窄或阻塞情况及其程度,从而有利于诊断和选择治疗方案。
Sher曾用MRI检查证实患有OSAHS的患者较同样肥胖而无OSAHS者在咽腔塌陷周围区域有较多的脂肪聚积;因此,MRI的动态检查技术也适用于本征的检测。
(四)多导睡眠监测法
多导睡眠监测法(polysomnography,PSG)是诊断睡眠呼吸紊乱疾患最重要的技术手段,也是睡眠实验室不可缺少的监测设备。早期是利用多用脑电图机将脑电、眼动、肌电、心电、口鼻气流、胸腹呼吸运动等信号同步记录在记录纸上,再对记录纸上的这些信号进行分析、统计。随着传感技术、计算机技术、数字技术及网络技术的发展,现今PSG监测已有了很大的发展,这表现在:①实现了无纸化记录,可将数据直接储存在硬盘中,并可转存到光盘、可移动磁盘、磁带等储存介质中长期保存,储存量大且占用空间小,易于检索资料;②实现了同步红外摄像监控,大多数的PSG系统都配备有红外摄像系统,值班人员在中心监控室可对多台仪器进行监控,可减少对患者睡眠的干扰,且影像资料与其他数据可同步传输,便于分析数据及了解患者监测时的情况,可有效地节约人力成本;③采用了数字化处理技术,PSG系统获得的信息经数字化处理后,可减少容量,加快传输速度、减少失真率、降低传输距离及其他干扰的影响,可大大提高计算机辅助诊断的准确率;④实现了信息化和智能化,计算机软件开发的日益成熟,使其辅助诊断的准确率越来越高,除可对睡眠结构、呼吸、血氧等常规参数进行分析、测量外,还能提供许多既往依靠人工方法无法获得的数据,如脉搏传递时间,脑电频谱分析等,使人们对睡眠呼吸紊乱易于获得更多新的认识;⑤可与互联网连接,进行在线远程监测、浏览、分析及会诊,医师可在自己的计算机上对远程资料进行采集和分析,并与异地医师交流、讨论,实现远程医疗及医疗资源共享。此外,PSG系统还可在必要时根据需要扩充、增加外接设备及软件升级。
新型的PSG系统主要由监测床、传感器、前置放大器、红外线摄像系统、计算机辅助系统等组成,其基本工作原理是:不同的传感器将机体信号收集起来,将干扰滤过后经前置放大器将信号放大,再通过模—数转换器将模拟信号转换成数字信号,经电缆线传输到计算机里,同时红外摄像系统可将受试者的影像资料同步传输至计算机,这些信号在监视器下同步显示并储存在计算机硬盘里,通过计算机辅助软件系统实时或事后对记录信息进行初步分析后再经专业人员校正,即能获得快速而准确的分析结果。
大多数PSG系统可监测的参数如下
1.脑电(electroencephalogram,EEG)
EEG信号为低振幅电位(微伏级),由位于大脑皮层的锥体细胞产生,极化和去极化响应不同的刺激,产生EEG波形。这些波动的电位被置于头皮的电极探测到,经信号放大后显示或记录在PSG系统里,用以判定睡眠开始和觉醒。
2.眼动(electro-oculogram,EOG)
眼球活动时,角膜与视网膜位置的改变可以导致电位差的改变,以安放在靠近角膜的电极为正极,靠近视网膜的电极为负极,在PSG上可记录到一次眼动波形。
3.肌电(electromyogram,EMG)
由肌肉收缩而产生的动作电位,一般记录到的肌电频率范围为20~5000赫兹,振幅为20微伏至50毫伏。PSG系统的EMG通过安放在拟监测肌群皮肤上的表面电极获得,为双极记录。在标准的PSG监测上,颏下肌的EMG用于REM睡眠分期的标准;胫前肌EMG用于评价患者是否有周期性腿动;肋间肌EMG用于监测呼吸努力(奋力)。
4.心电(ECG)
ECG监测是通过检测心电活动时显示在皮肤上的大约1微伏的小电压。几个电极按照标准导联放置在皮肤上以感知这些电压,1个ECG导联需要两个以上电极,第3个电极作为参照以减少电干扰。ECG的时间间隔和波形可提供患者的心率的快慢、是否有心律不齐或其他异常。
5.肺容积变化
(1)变形测量计
通常由注满可通过电流的导体的密封弹性小管做成,当长度改变时,其电流及电阻也相应发生改变,通过多元线性回归技术可得到每个传感器的标定因子。通常将2经过标定的个测量计分别置于胸廓和腹部,用于定性检测呼吸异常及定量测量动态容积变化。
(2)感应性体积描记仪
传感器都由一个缝在经过弹性化处理的带子上水平方向呈正弦形状的绝缘电线构成,将其置于导电性相同的胸廓及腹部,当肺容积改变时,胸廓及腹部横切面的大小亦随之变化,从而改变每个传感器的直径,其自感应系数的变化即可测得。
(3)阻抗式呼吸描记仪
将一对电极置于胸廓活动度最大的部位(通常就通过ECG导联的两个电极),并用10~100千赫兹的载频正弦恒流向人体加以0.5~5微安的安全电流,从而在相同的电极上获取呼吸阻抗变化的信号。这种呼吸阻抗的变化图描述了呼吸的动态波形,并可提取呼吸频率参数。
6.气流监测
(1)鼻气流压力
吸气时气道压力低于大气压,呼气时,气道压力高于大气压,因此,测量呼吸时鼻气流压力的变化即可反映气流的大小。
(2)热敏传感器
热敏传感器置于口鼻气流通过处,呼出气加热传感器使其电阻增加,吸入气使传感器温度降至室温,电阻减少,其变化被记录下来,即可反映呼吸情况。
(3)呼气末CO2(ETCO2)
有主流式和旁流式测量方法,主流式直接将气体传感器置于患者的呼吸气路导管中,直接对呼吸气体中的CO2进行浓度转换,然后将电信号传入监测系统进行分析处理,得到ETCO2参数;旁流式的光学传感器置于监测仪内,由气体采样管实时抽取患者呼吸气体样品,送入监测仪进行CO2浓度分析。
7.脉搏血氧监测(SpO2)
将含有两个LEDs(发光二极管)的探头放在患者的指尖、耳垂或足尖,可测出患者的SpO2值。
8.其他
PSG还可测量血压、鼾声、食管压力及夜间阴茎勃起功能等。
PSG通过对以上内容的监测分析,可以得到的参数包括总记录时间,总睡眠时间,睡眠效率[TST/TRT(%)],Ⅰ+Ⅱ期睡眠/TS(%),Ⅲ+Ⅳ期睡眠/TST(%),快动眼(REM)睡眠/TST(%),打鼾时间(snoring time,ST)比[ST/TST(%)],呼吸暂停低通气指数 (apnea hypopnea Index,AHI),最低指脉氧饱和度(LSpO2)等,据此可判定OSAHSD的类型及严重程度。
(五)听性脑干反应测试
Synderman等(1982)对睡眠呼吸暂停综合征患者进行ABR测试,发现23例成年患者中,中枢型者都有波Ⅴ延长,而阻塞型与混合型也有异常的脑干诱发电位,但无特殊构型。Wetmore等(1988)测试 27例 OSAHS患者,术前ABR各参数与对照组比较未发现有统计学意义的改变,而与术后相比显示了波Ⅲ潜伏期及波Ⅰ~Ⅲ间期延长。Peled等比较了OSAHS患者白天清醒状态下与夜间呼吸暂停不同发作相之间的ABR,未发现有意义的改变。倪道凤等观察了20例OSAHS患者的ABR变化,发现波Ⅰ、Ⅴ潜伏期及波Ⅲ~Ⅴ间期延长、波Ⅰ~Ⅲ间期缩短、波Ⅲ潜伏期及波Ⅰ~Ⅴ间期在正常范围内;提示OSAHS对耳蜗和听觉脑干结构均有影响,但对各部位的影响不尽相同。
(六)其他检查
如儿童病例可在睡眠期间取血检测生长激素浓度;甲状腺功能低下者行甲状腺功能检测;肢端肥大症者除典型面貌、肢端肥大等全身征象外,尚可行蝶鞍区、指端骨及其他颅骨、长骨、脊椎骨X线拍片或CT扫描等;并与有关各科会诊以确定诊断,明确本征相关病因。
根据病史及上述检查,尤其是多导睡眠图监测的结果,可对本征做出诊断。诊断中要力争弄清咽部塌陷的部位,以便为选择治疗方案尤其是手术治疗提供依据。诊断中还应注意与下列疾病相鉴别
1.婴儿猝死综合征
外观健康的婴儿,大多于睡眠期间突然意外死亡,原因不清。通常发生于3周至5~6个月的婴儿,几乎不发生于2周之前和8个月之后,具有特色性的年龄分布。冬天易发生,多见于男孩,有的婴儿死亡可能与上呼吸道感染、喉炎、喉痉挛、鼻塞等以及体重较轻有关。也有人认为OSAHS可能为SIDS的致死原因之一。但OSAHS多发生于中年以上的男性,睡眠时鼾声等症状明显,多可发现病因,故鉴别不甚困难。
2.发作性睡病
间断发生的突然嗜睡或无法控制睡意的状态,可伴有猝倒。发病年龄多在14~16岁,30岁以后发病者很少;男多于女,男女之比约为1∶0.62。发作时可突然哈欠不断,侧身便睡;入睡10~20分钟,醒后一切如常人,但过数小时又可能再次发作。本病发病年龄较轻,无呼吸梗阻等病症,易与OSAHS鉴别。











