英文名称 :intracranial hemorrhage
新生儿颅内出血(neonatal intracranial hemorrhage,ICH),是新生儿期最常见的神经系统疾病,其发病率为20%~30%,胎龄和出生体重不同,其发病率差别较大。新生儿颅内出血与其自身的解剖特点和围生期高危因素有关,可发生不同部位的出血,主要类型有脑室周围-脑室内出血(subependymal hemorrhage-intraventricular hemorrhage,SEH-IVH)、硬 膜 下 出 血(subdural hemorrhage,SDH)、蛛网膜下腔出血(subarachnoid hemorrhage,SAH)、脑实质出血,以及小脑及丘脑、基底核出血等。随着围产技术及新生儿重症监护水平的提高,目前足月儿颅内出血的发病率已明显降低,早产儿颅内出血特别是脑室周围-脑室内出血已成为主要出血类型,占新生儿颅内出血的80%以上。
(一)脑室周围-脑室内出血
脑室周围出血即室管膜下出血(SHE),也称生发基质出血,当出血量增加,室管膜破溃,血液流入脑室则形成脑室内出血(IVH)。多种因素可致早产儿发生SHE-IVH,同一患儿常常是多种病因共同作用而发病。
1.脑血管血管发育不成熟
胎龄小于32周的早产儿,在脑室周围的室管膜下留存胚胎生发基层,其血管丰富,为不成熟的毛细血管网,血管壁仅有一层内皮细胞,缺少胶原和弹力纤维支撑,当动脉压突然升高时可导致毛细血管破裂引起室管膜下出血,出血向内穿破室管膜进入脑室内引起 IVH,血液外渗可扩散至脑室周围的白质。生发基质层血管壁内皮细胞富含线粒体,耗氧量大,缺氧易发生管壁破坏出血。此外,Monro孔水平室管膜下区域深部静脉循环成独特的“U”形,是生发基层血管和静脉循环之间的唯一解剖通道,在增加颅内压方面起重要作用,易因血流动力学的变化而导致出血及出血性脑梗死。
2.压力被动性脑血流
颅内压改变是颅内出血的直接原因,其高低与脑血流量密切相关,特别是“涨落”型脑血流,颅内压随之上下波动,与颅内出血关系密切。新生儿特别是早产儿脑血管自主调节功能不完善,在内外环境发生变化时,颅内压不能维持在相对稳定的水平,这种现象被称为“压力被动性脑血流”。全身血流变化时脑血流量随之变化,脑血流涨落 > 10%就有发生出血的可能。引起脑血流涨落的原因很多,如脐静脉插管、机械通气、高碳酸血症、低血容量、低血压、动脉导管未闭、低血糖、吸入高浓度氧等。
3.血液因素
新生儿的血小板活性明显低于成人,生后3~4天尤为明显,10~14天才接近成人水平,这与IVH多发生在生后3天内相吻合。早产儿血小板数目低也可能是其发生IVH的重要原因之一。新生儿肝功能不成熟,体内凝血因子Ⅱ、Ⅶ、Ⅸ、X活性较低,凝血机制不健全。早产儿凝血因子水平普遍降低,抗凝血酶Ⅲ、蛋白C、纤溶酶原和抗纤溶酶等明显低下,从而导致颅内出血的发生增多。
(二)硬膜下出血
硬脑膜是一层分隔大脑的厚膜。静脉窦位于硬脑膜反折的褶皱中,硬脑膜撕裂可能会造成静脉窦破裂,导致广泛的硬脑膜内和硬膜下出血。来自硬脑膜的交通静脉到达矢状窦,这些血管破裂也会导致SDH。常发生于巨大儿、头大、胎位异常难产或高位产钳助产的新生儿。SDH因交通静脉破裂、扭曲力/颅骨异位(骨分离)造成的硬脑膜撕裂所致,颅骨异位还可致小脑出血。
(三)蛛网膜下腔出血
分为原发性和继发性出血。原发性SAH指出血原发部位在蛛网膜下腔,在新生儿多见,与缺氧、酸中毒、低血糖、产伤等因素相关,因蛛网膜下腔的交通静脉、软脑膜下血管破裂出血所致。继发性SAH是指其他部位的出血进入蛛网膜下腔,包括硬膜下、脑室内、小脑等部位的出血向蛛网膜下腔的扩展;也可以是动脉梗死区域上方发生SAH。
(四)脑实质出血
此类出血程度差异大,病因不同,大致分以下几种情况。
1.足月儿脑实质出血
(1)梗死:
分动脉性或静脉性梗死,由此并发的出血往往涉及多个部位,可能是产时的窒息、凝血功能障碍等所致。动脉性梗死最常见于大脑中动脉,而更多的脑实质出血是静脉性梗死,常是由脑室下静脉引流区静脉血栓所致的单侧颞叶局灶性出血,即通常所说的点片状出血。
(2)凝血缺陷病:
凝血因子异常、α1-抗胰岛蛋白酶缺乏、维生素K1缺乏是引起足月儿脑实质出血最重要的原因。
(3)体外膜氧合(ECMO):
目前已知脑实质出血是ECMO的重要并发症。因在ECMO时必须给予抗凝药物,置管导致颈动脉血流受影响致缺血进而继发出血,或ECMO引起静脉窦血栓形成发生脑实质出血。
(4)脑血管畸形:
动脉瘤、动静脉畸形以及肿瘤是足月儿脑实质出血的少见原因。
2.早产儿脑实质出血
早产儿严重的颅内出血可伴有脑实质多处出血,多发生在孕周和出生体重很小的早产儿,出血的原因可能与严重疾病和特殊治疗状态下的出凝血机制以及脑血流动力学的极度变化有关。
(五)小脑出血
有原发性小脑出血,也可是其他部位出血扩展而来,早产儿多见。第四脑室底部生发基质中的血管容易受损出血进入小脑皮质。臀位分娩时枕骨分离致小脑创伤也是常见出血原因。
(六)丘脑、基底核区域出血
大脑中动脉于颅底水平段发出的豆纹动脉分支供应丘脑、基底核,这些血管很细,与主干血管呈90°夹角,很易受血流动力学的影响而破裂出血。
随着产科监护技术的进步,足月儿产伤性新生儿颅内出血已显著减少,但早产儿缺氧性新生儿颅内出血发生率仍高。早产儿新生儿颅内出血发生率,国外报道为20%,国内报道为40%~50%,病死率为50%~60%。
1.产伤性颅内出血
多见于足月儿。由于分娩过程中头颅受力不均或受力过大而使大脑帘及小脑幕撕裂引起。
2.缺氧缺血性颅内出血
缺氧缺血损伤脑血管自主调节功能,形成压力被动性脑血流,当体循环压力升高时,脑血流量增加,导致毛细血管破裂出血。
3.凝血功能障碍
多见于新生儿出血症,先天性凝血因子缺乏及严重感染、弥漫性血管内凝血的患儿。
1.硬脑膜下出血
见于有难产史足月儿。症状轻重与出血部位及出血量有关。大脑镰撕裂或小脑幕下大量出血可压迫延髓生命中枢,生后很快出现抑制状态,出现嗜睡、昏迷、呼吸不规则或暂停,各种生理反射消失,最后出现呼吸衰竭死亡。限局性大脑表浅静脉破裂轻微出血者可无症状,血肿可自行吸收或形成慢性血肿,压迫其下脑组织形成局灶性癫痫。后颅窝硬脑膜下血肿可有神经系统症状和体征,但无前囟饱满及颅缝分离表现。
2.蛛网膜下腔出血
多为缺氧引起毛细血管内血液外渗,亦可为脑室内出血或硬脑膜下出血时,血液流入蛛网膜下腔所致。出血量少者可无症状,重症可从兴奋转为抑制状态,反复惊厥较为多见,大量出血者可很快死亡,血性脑脊液为其特点,存活者易有脑积水。
3.脑室周围-脑室内出血
多见于早产儿。胎龄愈小,发病率与病死率愈高。症状轻重不一。出血量少者可无症状和体征。严重者以死胎娩出,或娩出后难以建立呼吸,或生后24小时内出现症状,由兴奋转为抑制,病情急剧进展而死亡。幸存者常有阻塞性脑积水。
4.小脑出血
多见于早产及极低出生体重儿,大部分为病情急剧恶化,常在生后12~36小时之内死亡。
1.硬膜下出血(subdural hemorrhage)
硬膜下出血多见于足月儿,主要由产伤引起,虽然不太常见,但是新生儿期颅内出血中较严重的一种,出血量多时可导致休克而死亡。
大脑的深部静脉在大脑镰与小脑幕交界处流入Galen(盖仑)大静脉,Galen静脉与位于大脑镰下缘的下矢状窦融合形成直窦。直窦向后走行与位于大脑镰上缘的上矢状窦汇合形成横窦。位于小脑幕侧缘的横窦血最后流入颈静脉。大脑表面的静脉血通过脑表面桥静脉引流入上矢状窦静脉。新生儿硬膜下出血主要包括:小脑幕撕裂,枕部骨分离,大脑镰撕裂和大脑表面桥静脉破裂。
(1)小脑幕撕裂
小脑幕撕裂通常引起Galen(盖仑)静脉,或直窦,或横窦及幕内静脉破裂,有研究提示:幕内动脉也可能破裂。出血最常发生于幕下,可流进后颅窝,当出血量多,速度快时,血凝块压迫脑干,导致死亡。随着现代脑影像检查技术的进步,目前,已知轻度小脑幕撕裂比严重的小脑幕撕裂更常见,它包括幕下出血和幕上出血。另外,出血可仅局限于小脑幕游离缘,最常见在小脑幕与大脑镰交界附近,或进一步向前扩展进入蛛网膜下腔,或脑室系统。
(2)枕骨分离
产钳分娩所引起的严重产伤是枕骨分离,伴后颅窝硬膜下出血和小脑撕裂。严重时硬膜和枕部静脉窦被撕裂,导致颅后窝大量出血和小脑撕裂。
(3)大脑镰撕裂
大脑镰撕裂常发生于大脑镰与小脑幕交界处。单纯大脑镰撕裂比小脑幕撕裂少见。出血常来自于下矢状窦,凝血块位于胼胝体上大脑纵裂。
(4)脑桥静脉破裂
脑表面脑桥静脉破裂导致大脑表面出血,即脑表面硬膜下出血。血肿在脑表面两侧常常比在上矢状窦附近更广泛。当出血量较多时,多为单侧性,且伴有蛛网膜下腔出血。脑表面硬膜下出血相对较常见,特别是在足月儿尸解中。导致脑表面硬膜下出血的产伤常常也引起脑钝挫伤。
2.原发性蛛网膜下腔出血
原发性蛛网膜下腔出血(primary subarachnoid hemorrhage)指蛛网膜下腔内的出血,而不是继发于硬膜下、脑室内、或颅内的出血扩展进入蛛网膜下腔。主要与产伤或缺氧有关。
蛛网膜下腔出血的血液通常位于大脑表面,特别是后部以及后颅窝。在临床未怀疑蛛网膜下腔出血的新生儿尸解中,小量的蛛网膜下腔出血经常被发现。
3.脑室内出血
脑室内出血(intraventricular hemorrhage,IVH)足月儿脑室内出血的神经病理不同于早产儿,早产儿的IVH出血主要来自室管膜生发层基质,而足月儿IVH出血主要来自脉络丛,特别常见的出血部位是其球后部。少数足月儿脑室内出血出血来自室管膜下生发层基质,特别是丘脑-尾状核沟部位的室管膜下生发层基质,这个部位的生发层基质在新生儿期最后消失。轻度脑室内出血一般不产生并发症,严重的脑室内出血晚期合并出血后脑积水(posthemorrhagic hydrocephlaus)。
4.脑实质出血
(1)小脑出血
小脑出血主要有三种类型:原发性小脑出血,脑室内出血或蛛网膜下腔出血扩展进入小脑,及产伤引起小脑撕裂。出血既可在小脑半球也可在蚓部,出血严重时,小脑皮质和白质均被破坏,足月儿小脑蚓部出血多见。另外,软脑膜下,外颗粒细胞层表面的生发层基质,及第四脑室室管膜下生发层基质的少量出血也常见。
(2)基底节和/或丘脑出血
基底节和/或丘脑出血多伴有坏死,单纯的基底节和/或丘脑出血较少见,一般为单侧,少数为双侧。
(3)大脑皮质出血
主要有散在点或片状出血,大脑某一主要动脉或静脉梗死出血及严重脑室内出血穿破室管膜进入脑实质,在足月儿,前两种出血多见。
(4)脑白质出血
主要有严重脑室内出血穿破室管膜进入脑白质,脑室周围白质软化并发梗死出血,散在点或片状出血。白质出血多见于早产儿。
1.机械损伤
各项产伤因素均可致胎儿头部在分娩过程中骤然受压或过度牵引,使颅骨过度变形,引起大脑镰等撕裂出血。
2.凝血功能未成熟
由于凝血因子不能经母‐胎转运,须由胎儿未成熟的肝脏合成,故新生儿生后1周内血浆大多数凝血因子水平不足,其中4个维生素K依赖因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ)和4个接触因子(Ⅺ、Ⅻ、PK、HMWK)仅为成人的50%,Ⅴ因子、Ⅷ因子虽高,但半衰期短而不稳定,Ⅰ因子水平与成人接近,但因存在胎儿纤维蛋白原,含较多唾液酸而活性弱,转化为纤维蛋白较慢。此外,新生儿抗凝血酶Ⅲ(AT‐Ⅲ)活性亦低下,血小板也处于低值。由于新生儿凝血物质不足,抗凝活性低下,故常有生理性出血倾向并致出血难止,早产儿尤甚。
3.脑血管发育不成熟
(1)血管缺乏基质保护
生发基质位于侧脑室底的室管膜下,其最突出部分位于尾状核头部,从侧脑室前角延至颞角、第三、四脑室顶部。胎龄26~32周,侧脑室生发基质区和脉络丛微血管基质发育滞后于脑实质其他部位,部分早产儿细胞外基质Ⅳ型胶原纤维、黏连蛋白和纤维连结蛋白含量少,致无连续完整基膜。侧脑室生发基质于胎龄32周后才逐渐萎缩,而脉络丛微血管膜亦于足月后才发育成熟。在此期间,侧脑室生发基质区的血管密度和面积明显高于白质区,尽管周围微血管丰富,但因缺乏基质保护,由单层内皮细胞所组成的、缺少平滑肌及弹力纤维支持的血管,对抗血流冲击能力差,在缺氧、缺血、酸中毒、脑血流速波动等影响下,生发基质区易发生破裂出血。随着孕龄的增加,出血多来自脉络丛。
(2)长穿支血管少
在脑血管发育过程中,脑皮层血液供应来自软脑膜动脉,有较好的侧支循环,供应皮层下白质区为动脉的短穿支,均不易发生缺血性损害。供应脑室周围深部白质为动脉长穿支,早产儿越不成熟,长穿支越少,且缺少侧支循环,一旦缺血,该区最易受损。
(3)血管呈U字形曲折
脑白质引流的静脉通常呈扇形分布于脑室周围白质,在脑室旁经生发基质区汇入终末静脉,此静脉在侧脑室马氏孔后方、尾状核部前方呈U字形曲折,汇入大脑内静脉。当静脉压增高时,血液回流受阻,U字形曲折处压力升高,易发生充血、破裂出血或出血性梗死。
4.脑血流波动
(1)被动压力脑循环
指脑血流随血压的变化而变化的形式。早产儿脑室周围循环血流分布不匀,存在高容量血流区和侧脑室生发基质低容量血流区,该区血流量极低,每100g脑组织血流量<5ml/min,而正常脑血流量为每100g脑组织40~50ml/min。早产儿脑血管自主调节功能差,调节范围窄,因此,各种原因引起的脑血流改变,均可导致新生儿颅内出血H。
(2)脑血管对二氧化碳敏感
CO2每增加1mmHg,脑血管扩张导致脑血流增加8.6%,若PaCO2增加过多,超过脑血管扩张极限,可致血管破裂出血。反之若PaCO2减少,则脑血管收缩,脑血流减少,使低血容量区缺氧缺血,导致血管变性或缺血再灌注损伤,同样亦会引起新生儿颅内出血。
鉴于临床诊断的许多不确定因素,影像学检查成了新生儿颅内出血诊断的确诊方法。可确定颅内出血的类型,并对出血程度作出评判。
1.头颅B超
头颅B超用于诊断ICH及其并发症,其敏感性及特异性分别高达96%及94%,可床旁检查,无辐射,是检查ICH的首选方法。因ICH多在生后1~7天内发生,故首次检查宜在此时进行,每隔7~14天复查1次,出血稳定后仍须定期检查有否发生出血后脑积水。超声(US)对诊断 SHE 和 IVH 的敏感性最高,因US对颅脑中心部位分辨率高、对低血红蛋白浓度具有较高敏感性。脑室少量出血、脑脊液中血细胞比容低至0.2%、出血吸收期血红蛋白降至70~80g/L,出血部位与周围组织密度相等时US仍可分辨并作出诊断,CT却难以发现,因此头颅B超在很大程度上代替CT检查。
SEH-IVH的头颅B超表现及诊断标准,按Papile分级法分为4级:Ⅰ级,单或双侧室管膜下生发基质出血。Ⅱ级,室管膜下出血穿破室管膜引起脑室内出血,但无脑室增大。Ⅲ级,脑室内出血伴脑室扩大,可测量旁矢状面侧脑室体部最宽纵径,6~10mm为轻度扩大,11~15mm为中度扩大, > 15mm为重度扩大;也可由内向外测量旁矢状面脑室后角斜径, ≥ 14mm为脑室扩大;可每次测量脑室扩大的同一部位动态评估。Ⅳ级,脑室内出血伴脑室周围出血性梗塞。
2.头颅CT
可用于各部位颅内出血的诊断,一般在生后1 周内检查。其SEH-IVH分级与B超相同,但分辨率明显逊于US,对室管膜下及少量脑室内出血敏感性亦不及US。分辨率及对脑实质病变性质的判断不及磁共振显像。7~10天后随着出血的吸收血红蛋白逐渐减少,CT 中出血的密度也逐渐降低至与周围组织相近,因此对残余积血不敏感。因CT的高辐射性,现很少用于新生儿颅内出血的诊断。
3.头颅磁共振显像(MRI)
对各种类型的出血均有较高诊断率,分辨率高于头颅B超与CT,並可准确定位,同时可明确有无脑实质损伤。但对新鲜出血敏感性较差,宜在出血3天后检查。因新鲜出血主要为氧合血红蛋白,T1加权像上仅表现为等信号或稍低信号,在T2加权像上表现为高信号。7~10天后,氧合血红蛋白渐变为脱氧血红蛋白和高铁血红蛋白,在MRI 中的信号也随之变化,T1 和T2 加权像上均表现为高信号。因此,通过MRI中的出血信号还可以初步估计出血时间。
CT和MRI可很好辨别第三、第四脑室内出血以及SDH和SAH,但US不能,因US对颅脑边缘及后颅窝部位的病变分辨率差。大量的脑实质出血,小脑和丘脑、基底核出血,US、CT 和MRI均能作出明确诊断(表1)。
表1US、CT和MRI对各种颅内出血的诊断效果
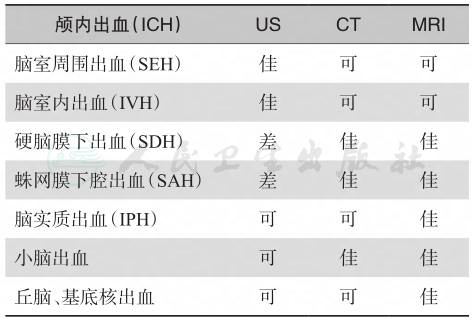
引自:儿科急诊医学(第5版).第5版.ISBN:978-7-117-33028-2.主编:
4.脑脊液检查
在20世纪70年代以前,临床医师经腰穿诊断新生儿颅内出血,急性期脑脊液为均匀血性,红细胞呈皱缩状,糖定量降低且与血糖比值 < 0.6(正常0.75~0.80),蛋白升高。但目前临床已不采用,因此法为有创检查,仅能反映脑室内、蛛网膜下腔出血;出血量多时才有异常,出血量与脑脊液中红细胞数无关联。
1.耐心讲解病情,减轻家属不良情绪。
2.有后遗症者,建议康复训练及随访。
1.产前预防
(1)预防早产,预防可导致产伤的各种因素,治疗孕产妇高危疾病如妊娠期高血压病。
(2)早产孕妇产前应用糖皮质激素:糖皮质激素在促肺成熟的同时,亦可促进生发基质毛细血管发育成熟,明显降低新生儿ICH的发生率。
(3)早产孕妇产前应用维生素K1:可提高胎儿血浆Ⅱ、Ⅶ、Ⅹ三种凝血因子水平,从而降低早产儿颅内出血发生。于分娩前维生素K1注射,用一次即可。
2.产时预防
建议延迟结扎脐带,已证实早产儿分娩后至少60秒再结扎脐带,与10秒内结扎脐带比较,早产儿颅内出血发生率明显降低。
3.产后预防
尽可能维持较稳定的颅内压和脑血流量,避免“涨落”现象。使用呼吸机尽量避免过高的吸气峰压及人机不同步。尽量不使用高渗液体,护理患儿时动作轻柔,减少干扰,保持安静、避免剧烈哭闹,保持头高位15°~30°。
4.药物预防
(1)苯巴比妥:
曾有报道早产儿应用苯巴比妥后,脑室内出血、重度脑室内出血发生率下降。作用机制是降低脑代谢率,降低颅内压,通过镇静和抗惊厥作用减少血压波动。但循证医学证据认为,此法对降低ICH及ICH后遗症、病死率均无效,且可增加对机械通气的需求,因而不推荐使用。
(2)吲哚美辛:
能调节脑血流、促进室管膜下生发基质成熟。出生体重 < 1 250g之早产儿,于生后6~12小时给予吲哚美辛0.1mg/kg,24小时后重复1次或首剂后每12小时1次,连用2~3天,脑室内出血发生率降低66%。但因其有降低各重要脏器血流灌注和影响血小板聚集等不良反应,临床未将其作常规预防药物。











