去看看
去看看


一、概述
淋巴瘤(lyphoma)是我国最常见的恶性肿瘤之一。根据国家癌症中心公布的数据,2014年我国淋巴瘤的确诊发病率为5.94/10万,2015年预计发病率约为6.89/10万。由于淋巴瘤病理类型复杂,治疗原则各有不同,为进一步提高淋巴瘤诊疗能力和规范化水平,配合抗肿瘤药品供应保障有关政策调整,保障医疗质量与安全,现对《中国恶性淋巴瘤诊疗规范(2015年版)》进行修订和更新。
二、淋巴瘤的诊断
应当结合患者的临床表现、体格检查、实验室检查、影像学检查和病理学等进行诊断。
(一)临床表现
淋巴瘤的症状包括全身和局部症状。全身症状包括不明原因的发热、盗汗、体重下降、皮肤瘙痒和乏力等。局部症状取决于病变不同的原发和受侵部位,淋巴瘤可以原发于身体的任何器官和组织,通常分为原发于淋巴结和淋巴结外两大类。最常见表现为无痛性的进行性淋巴结肿大。如有以上述症状的患者在基层医院就诊时,应予以重视,并尽早转诊至上级医院或肿瘤专科医院。
(二)体格检查
应特别注意不同区域的淋巴结是否增大、肝脾的大小、伴随体征和一般状态等。
(三)实验室检查
应完成的实验室检查包括血常规、肝肾功能、乳酸脱氢酶(lactate dehydrogenase,LDH)、β2微球蛋白、红细胞沉降率、乙型肝炎和丙型肝炎病毒检测以及骨髓穿刺细胞学和活检等,还应包括人类免疫缺陷病毒(human immunodeficiency virus,HIV)筛查在内的相关感染性筛查。对原发胃的黏膜相关边缘带B细胞淋巴瘤,应常规进行幽门螺杆菌(helicobacter pylori,Hp)染色检查;对NK/T细胞淋巴瘤患者,应进行外周血EB病毒DNA滴度检测。对于存在中枢神经系统受累风险的患者应进行腰穿,予以脑脊液生化、常规和细胞学等检查。
(四)影像学检查
常用的影像检查方法:计算机断层扫描(computed tomography,CT)、核磁共振(nuclear magnetic resonance,MRI)、正电子发射计算机断层显像(positron emission tomography,PET-CT)、超声和内镜等。
1. CT:目前仍作为淋巴瘤分期、再分期、疗效评价和随诊的最常用影像学检查方法,对于无碘对比剂禁忌证的患者,应尽可能采用增强CT扫描。
2. MRI:对于中枢神经系统、骨髓和肌肉部位的病变应首选MRI检查;对于肝、脾、肾脏、子宫等实质器官病变可以选择或者首选MRI检查,尤其对于不宜行增强CT扫描者,或者作为CT发现可疑病变后的进一步检查。
3. PET-CT:目前是除惰性淋巴瘤外,淋巴瘤分期与再分期、疗效评价和预后预测的最佳检查方法。对于下列情况,有条件者推荐使用PET-CT:①PET-CT可作为霍奇金淋巴瘤(Hodgkin lymphoma,HL)以及 氟脱氧葡萄糖(fluorodeoxyglucose,FDG)亲和性高的非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)亚型治疗前分期以及再分期的常规检查,并用Deauville五分量表(表1)评估病变缓解情况。但对于FDG亲和性差的淋巴瘤亚型(如惰性淋巴瘤),治疗前的分期检查仍以增强CT扫描为首选。②如果有影像学的临床指征,PET-CT 可用于治疗中期疗效评价,但仍处于临床研究阶段,故根据中期PET-CT结果更改治疗方案仍须慎重。③对于HL和多数弥漫性大B细胞淋巴瘤(Diffuse large B cell lymphoma,DLBCL),如果PET-CT提示有明确的骨髓受累,则无需行骨髓活检。④PET-CT可以作为惰性淋巴瘤向侵袭性更强的病理类型转化时活检部位选择的依据。= 5 \* GB3⑤PET-CT对于疗效和预后预测好于其他方法,可以选择性使用。
4. 超声:可用于浅表淋巴结和浅表器官(如睾丸、甲状腺、乳腺等)病变的诊断和随诊,但一般不用于淋巴瘤的分期诊断。对于浅表淋巴结和浅表器官(如睾丸、乳腺等)病变的诊断和治疗后随诊具有优势,可以常规使用;对于腹部、盆腔淋巴结检查可以选择性使用;对于肝、脾、肾、子宫等腹盆腔实质性器官的评估,可以作为CT和MRI的补充,尤其是不能行增强CT扫描时。在浅表淋巴结切除活检时,选取超声检测声像图异常的淋巴结,有助于提高活检的准确度。超声引导下穿刺活检也应用于深部淋巴结、肝脏、纵隔等部位的病变诊断。
5. 同位素骨扫描:淋巴瘤骨受侵患者的全身骨显像缺乏特征性改变,难以与骨转移瘤、多发性骨髓瘤、骨结核、骨纤维异常增殖症、甲状旁腺功能亢进、感染性疾病等鉴别,需要结合患者的病史、实验室检查和其他影像学检查。
常规骨扫描(99Tcm-MDP)对初治HL患者的临床评估价值有限,但骨扫描对原发骨淋巴瘤治疗后随访观察和预后评估作用优于CT。
(五)其他针对性检查
(1)可疑胃肠道受侵的患者应行胃镜、肠镜检查。
(2)常规进行心电图检查;有心血管基础疾病、高龄或拟应用蒽环类药物者选择性进行超声心动图检查。
(3)拟用博来霉素、且有肺基础病变者应进行肺功能检查。
(六)病理学检查
病理学检查是淋巴瘤诊断的主要手段。对于淋巴结病灶,应尽可能切除完整淋巴结。如果淋巴结病灶位于浅表,应尽量选择颈部、锁骨上和腋窝淋巴结。空芯针穿刺仅用于无法有效、安全地获得切除或切取病变组织的患者。初次诊断时,应首选切除或切取病变组织;对于复发患者,如果无法获得切除或切取的病变组织标本,可通过空芯针穿刺获取的病变组织进行病理诊断。
淋巴瘤的病理诊断需综合应用形态学、免疫组织化学(Immunohistochemistry,IHC)、遗传学和分子生物学技术以及流式细胞术等,尚无一种方法可以单独定义为“金标准”。
1.形态学:在淋巴瘤病理诊断中非常重要,不同类型的淋巴瘤具有特征性和诊断性的形态学特点。
2.IHC:可用于鉴别淋巴瘤细胞的免疫表型,如B或T/NK细胞、肿瘤细胞的分化及成熟程度等。通过组合相关的IHC标记物,进行不同病理亚型的鉴别诊断。
3.荧光原位杂交(fluorescence in situ hybridization,FISH)检测技术:可以发现特定的染色体断裂、易位或扩增等,对特定染色体异常相关淋巴瘤的辅助诊断有指导意义,如Burkitt 淋巴瘤相关的t(8;14)易位、滤泡性淋巴瘤相关的t(14;18)易位、结外黏膜相关淋巴组织边缘区淋巴瘤相关的t(11;18)易位、套细胞淋巴瘤相关的t(11;14)易位以及双打击或三打击高级别B细胞淋巴瘤相关的MYC(8q24)、BCL2(18q21)和BCL-6(3q27)重排等。
4.淋巴细胞抗原受体基因重排检测技术:淋巴细胞受体基因单克隆性重排是淋巴瘤细胞的主要特征,可用于协助鉴别淋巴细胞增殖的单克隆性与多克隆性,以及无法通过IHC诊断的淋巴瘤,是对形态学和IHC检查的重要补充。
5.其他:包括原位杂交、二代测序(Next-generation sequencing,NGS)、流式细胞技术等,是常规病理学诊断方法的有益补充。
随着新检测方法的出现,淋巴瘤的病理诊断也随病理研究的深入,出现新的改变。在2017年修订版WHO淋巴瘤分类中,间变大细胞淋巴瘤(anaplastic large cell lymphoma,ALCL)分为ALK 阳性ALCL、ALK 阴性ALCL和乳房植入相关的ALCL。ALK阴性ALCL的部分患者存在融合性突变,其中存在6p25染色体DUSP22和IRF4 重排的患者预后好,存在TP63重排的患者预后差;而血管免疫母细胞T细胞淋巴瘤(angioimmunoblastic T-cell lymphoma,AITL)与具有滤泡辅助性T细胞(follicular helper T cells,TFH)表型的结内外周T细胞淋巴瘤(peripheral T-cell lymphoma,PTCL),则被认为应归为一类。
三、淋巴瘤的分期
2014版Lugano会议对Ann-Arbor 分期系统进行了修订,适用于HL和原发淋巴结的NHL,而对于某些原发淋巴结外的NHL,如慢性淋巴细胞白血病、皮肤T细胞淋巴瘤、原发结外鼻型NK/T细胞淋巴瘤和原发胃、肠道、中枢神经系统淋巴瘤等,则难以适用,这些原发于特殊结外器官和部位的NHL,通常有其专属的分期系统。
四、淋巴瘤放射治疗
放射治疗是淋巴瘤综合治疗的重要组成部分,实施中如何选择放疗线束、射野和剂量,由具体病例的治疗目的和诊疗条件决定。可采用光子、电子和质子等射线束以达到对靶区的合理涵盖及正常组织的最大保护。复杂放疗技术如调强适形放疗(intensity modulated radiation therapy,IMRT)、屏气和呼吸门控、影像引导、甚至质子治疗,可在特定情况下,特别是在以治愈为目的预期生存期较长的患者中,显著提高临床获益,予以酌情推荐。
根据放疗目的和作用,淋巴瘤放射治疗的适应证分为:①根治性治疗;② 综合治疗的一部分;③ 化疗不能耐受或抗拒、残存病灶的挽救治疗;= 4 \* GB3④姑息治疗。
放疗设野分为:全淋巴照射(total lymphoid irradiation,TLI)和次全淋巴照射(sub-Total lymphoid irradiation,STLI)。TLI通常包括斗篷野+锄形野+盆腔野(在未行脾切除的病例中还需要进行脾照射),STLI可以省略部分受照区域,目前已不再用于HL综合治疗中。受累野照射(Involved field radiotherapy,IFRT)仅照射化疗前受累淋巴结的整个淋巴结区域,受累野范围包括所有已知肿瘤的部位和临近区域;随着影像诊断和适形放疗技术的发展,IFRT在HL和侵袭性淋巴瘤中,被更精准的累及淋巴结(involved-node radiotherapy ,INRT)或累及部位照射(involved-site radiotherapy ,ISRT)所替代。
附:
INRT:化疗前充分对肿瘤进行评估,在放射治疗体位下行PET-CT检查,并融合至化疗后放疗的定位CT中,准确照射所有化疗前大体肿瘤位置,即为INRT。该定义强调:一是射野就是化疗前大体肿瘤体积(Gross-tumor volume,GTV)的范围,二是必须有化疗前精确的治疗体位下的PET-CT评估。
ISRT:无法获取化疗前治疗体位下的PET影像时,可以通过适度增大射野来涵盖治疗中的不确定性因素。参考化疗前后的影像学信息,勾画出化疗前肿瘤位置,并外放一定边界对不确定性予以补偿。
ISRT靶区定义与勾画:
ISRT结内病变:目前ISRT作为化疗敏感的NHL和HL标准靶区勾画方法。计划需要以CT模拟为基础,融合其他现代显像手段如PET和MRI。ISRT的靶区主要目的是包括初诊时累及的淋巴结。射野包全化疗前或手术前最初的所有受累区域,但排除临近的正常组织,比如肺、骨、肌肉、肾脏等。化疗前或活检前GTV是勾画临床靶区(Clinical Target Volume,CTV)的基础。出于对存在疑问的亚临床病灶和对原始肿瘤显像准确性的考虑,可以在设置CTV时,基于临床判断适当扩充边界。对于惰性NHL,采用单纯放疗时,倾向采用扩大照射野。例如,FL的射野应该较同样受累时的DLBCL化疗后的射野更大。照射时在CTV基础上充分考虑器官运动形成的内靶区(internal target volume,ITV),之后形成计划靶区(planning target volume,PTV)。
ISRT结外病变:结外病变的射野原则与结内病变类似。但在某些结外器官原发病变中,CTV需要包括整个器官,如眼、乳腺、胃、唾液腺和甲状腺。在其他的结外器官中,如
附件1
2017年修订版WHO淋巴瘤分类






附件2
淋巴瘤的分期系统
附件2.1 Ann-Arbor(Cotswolds修订)分期系统
| Ⅰ期:侵及一个淋巴结区(Ⅰ),或侵及一个单一的淋巴结外器官或部位(ⅠE); Ⅱ期:在横膈的一侧,侵及二个或更多的淋巴结区(Ⅱ)或外加局限侵犯一个结外器官或部位(ⅡE); Ⅲ期:受侵犯的淋巴结区在横膈的两侧(Ⅲ)或外加局限侵犯一个结外器官或部位(ⅢE)或脾(ⅢS)或二者均有(ⅢES); Ⅳ期:弥漫性或播散性侵犯一个或更多的结外器官,同时伴有或不伴有淋巴结侵犯。 |
| A组:无全身症状; B组:有全身症状,包括不明原因发热(>38℃,连续3天及以上)、盗汗(连续7天及以上)或体重减轻(6个月内下降10%以上); E:淋巴瘤累及淋巴结外器官。单一结外部位受侵,病变侵犯到与淋巴结/淋巴组织直接相连的器官/组织时,不记录为Ⅳ期,应在各期后记入“E” 字母(如病变浸润至与左颈部淋巴结相连结的皮肤,记录为“IE”); X:大肿块,肿瘤直径>胸廓宽度的1/3或融合瘤块最大径>7.5cm。 |
附件2.2
慢性淋巴细胞白血病的Rai分期和Binet分期系统
Rai分期
| 分期 | 临床特征 | 危险分层 | 中位生存期(月) |
| 0 | 淋巴细胞增多,外周血淋巴细胞计数>15×109/L,且骨髓中淋巴细胞比例>40% | 低危 | >105 |
| Ⅰ | 0期,伴淋巴结增大 | 中危 | 101 |
| Ⅱ | 0~Ⅰ期,伴脾肿大、肝肿大或两者均有 | 中危 | 71 |
| Ⅲ | 0~Ⅱ期,伴血红蛋白<110g/L或红细胞压积<33% | 高危 | 19 |
| Ⅳ | 0~Ⅲ期伴血小板<100×109/L | 高危 | 19 |
Binet分期
| 分期 | 临床特征 |
| A期 | 血红蛋白≥100g/L,血小板≥100×109/L,受累淋巴结区域<3个 |
| B期 | 血红蛋白≥100g/L,血小板≥100×109/L,受累淋巴结区域≥3个 |
| C期 | 血红蛋白<100g/L和(或)血小板<100×109/L,,受累淋巴结区域不计 |
附件2.3
蕈样肉芽肿和Sézary综合征TNMB分期系统
| 皮肤 T1 | 局限性斑片、丘疹、和(或)斑块,<10%体表面积 |
| T2 | 斑片、丘疹、和(或)斑块,≥10%体表面积 |
| T3 | 一个或更多肿块形成(直径≥1cm) |
| T4 | 融合性红斑≥80%体表面积 |
| 淋巴结N0 | 无异常淋巴结;不需要活检 |
| N1 | 异常淋巴结;组织病理Dutch 1级或NCI LN 0~2 |
| N2 | 异常淋巴结;组织病理Dutch 2级或NCI LN 3 |
| N3 | 异常淋巴结;组织病理Dutch 3~4级或NCI LN 4 |
| NX | 异常淋巴结;无组织学确认 |
| 内脏 M0 M1 MX | 无内脏器官受累 内脏受累(须有病理学确诊和注明受侵器官) 内脏不正常;无组织学确诊 |
| 血液 B0 | 无明显血液受累:异型细胞(Sézary细胞)占外周血淋巴细胞比例≤5% |
| B1 | 低负荷血液受累:异型细胞(Sézary细胞)占外周血淋巴细胞比例>5%,但未达到B2水平 |
| B2 | 高负荷血液受累:异型细胞(Sézary细胞)≥1000/uL或CD4+/CD7-细胞比例≥40%或CD4+/CD26-细胞比例≥30% |
蕈样肉芽肿和Sézary综合征临床分期
| T | N | M | B | |
| ⅠA ⅡB | 1 2 | 0 0 | 0 0 | 0,1 0,1 |
| ⅡA ⅡB | 1~2 3 | 1,2 0~2 | 0 0 | 0,1 0,1 |
| ⅢA ⅢB | 4 4 | 0~2 0~2 | 0 0 | 0 1 |
| ⅣA1 ⅣA2 ⅣB | 1~4 1~4 1~4 | 0~2 3 0~3 | 0 0 1 | 2 0~2 0~2 |
附件2.4
Lugano胃肠淋巴瘤分期系统
| ⅠE期:病变局限于胃肠道; IE1:侵及黏膜、黏膜下层 IE2:侵及固有肌层、浆膜层 Ⅱ期:病变扩散至腹腔; II1:累及局部淋巴结 II2:累及远隔淋巴结 ⅡE期:侵透浆膜层达临近器官或组织; IV期:结外器官播散性受累或横膈上淋巴结受侵 |
附件3
淋巴瘤的预后评分系统
附件3.1 霍奇金淋巴瘤预后评分
早期霍奇金淋巴瘤不良预后因素
| 研究组 | 早期HL不良预后因素 |
| NCCN | 红细胞沉降率>50mm/h或伴B症状,肿块最大径/胸腔最大径>0.33或直径>10cm,受累淋巴结区>3个 |
| GHSG | 红细胞沉降率>50mm/h无B症状;红细胞沉降率>30 mm/h伴B症状,肿块最大径/胸腔最大径>0.33,受累淋巴结区>2个,有结外病变 |
| EORTC | 年龄≥50岁,红细胞沉降率>50mm/h无B症状;红细胞沉降率>30 mm/h伴B症状,肿块最大径/胸腔T5/6水平横径>0.35,受累淋巴结区>3个 |
| NCIC | 年龄≥40岁,混合细胞型或淋巴细胞消减型,红细胞沉降率>50mm/h或伴B症状,肿块最大径/胸腔最大径>0.33或直径>10cm,受累淋巴结区>3个 |
NCCN(National Comprehensive Cancer Network,美国国立综合癌症网络);GHSG(German Hodgkin Study Group,德国霍奇金淋巴瘤研究组);EORTC(European Organization for Research and Treatment of Cancer,欧洲癌症研究与治疗组织);NCIC(National Cancer Institute,Canada,加拿大国家癌症研究所)
晚期霍奇金淋巴瘤国际预后评分
(International Prognostic Score,IPS)
| 项目 | 0分 | 1分 |
| 白蛋白 | ≥40g/L | <40g/L |
| 血红蛋白 | ≥105g/L | <105g/L |
| 男性 | 否 | 是 |
| Ⅳ期 | 否 | 是 |
| 白细胞 | <15×109/L | ≥ 15×109/L |
| 淋巴细胞 | 占白细胞比例< 8%和(或)计数< 0.6×109/L | 占白细胞比例≥8%且计数≥0.6×109/L |
晚期霍奇金淋巴瘤国际预后评分与生存率
| 得分 | 5年无进展生存率(%) | 5年总生存率(%) |
| 0分 | 84 | 89 |
| 1分 | 77 | 90 |
| 2分 | 67 | 81 |
| 3分 | 60 | 78 |
| 4分 | 51 | 61 |
| ≥5分 | 42 | 56 |
附件3.2
弥漫大B细胞淋巴瘤预后评分
国际预后指数(International Prognostic Index,IPI)
| 项目 | 0分 | 1分 |
| 年龄(岁) | ≤60 | >60 |
| ECOG评分 | 0或1 | 2~4 |
| 临床分期 | Ⅰ或Ⅱ | Ⅲ或Ⅳ |
| 结外受侵部位数目 | <2 | ≥2 |
| LDH | 正常 | 升高 |
ECOG(Eastern Cooperative Oncology Group,美国东部肿瘤协作组);LDH(lactate dehydrogenase,乳酸脱氢酶)
| 风险分组 | 风险数 | 5年DFS | 5年OS |
| 低危 | 0或1 | 70% | 73% |
| 低-中危 | 2 | 50% | 51% |
| 高-中危 | 3 | 49% | 43% |
| 高危 | 4或5 | 40% | 26% |
DFS(disease free survival,无病生存期);OS(overall survival,总生存期)
修正的国际预后指数(Revised IPI,R-IPI)
| 项目 | 0分 | 1分 |
| 年龄(岁) | ≤60 | >60 |
| ECOG评分 | 0或1 | 2~4 |
| 临床分期 | Ⅰ或Ⅱ | Ⅲ或Ⅳ |
| 结外受侵部位数目 | <2 | ≥2 |
| LDH | 正常 | 升高 |
ECOG(Eastern Cooperative Oncology Group,美国东部肿瘤协作组);LDH(lactate dehydrogenase,乳酸脱氢酶)
| 风险分组 | 风险数 | 4年PFS | 4年OS |
| 预后非常好 | 0 | 94% | 92% |
| 预后好 | 1~2 | 82% | 82% |
| 预后差 | 3~5 | 45% | 58% |
PFS(progression free survival,无进展生存期);OS(overall survival,总生存期)
年龄调整的国际预后指数(age adjusted IPI,aaIPI)
| 项目 | 0分 | 1分 |
| ECOG评分 | 0或1 | 2~4 |
| 临床分期 | Ⅰ或Ⅱ | Ⅲ或Ⅳ |
| LDH | 正常 | 升高 |
ECOG(Eastern Cooperative Oncology Group,美国东部肿瘤协作组);LDH(lactate dehydrogenase,乳酸脱氢酶)
| 风险分组 | 风险数 | 5年DFS | 5年OS |
| 低危 | 0 | 56% | 83% |
| 低-中危 | 1 | 44% | 69% |
| 高-中危 | 2 | 37% | 46% |
| 高危 | 3 | 21% | 32% |
DFS(disease free survival,无病生存期);OS(overall survival,总生存期)
附件3.3
滤泡性淋巴瘤预后评分
滤泡性淋巴瘤国际预后指数(Folicullar lymphoma IPI,FLIPI)
| 项目 | 0分 | 1分 |
| 年龄(岁) | <60 | ≥60 |
| 血红蛋白水平 | ≥120g/L | <120g/L |
| 临床分期 | I或II | III或IV |
| 受侵淋巴结数目 | <5 | ≥5 |
| LDH | 正常 | 升高 |
LDH(lactate dehydrogenase,乳酸脱氢酶)
滤泡性淋巴瘤国际预后指数的风险分组与生存率
| 风险组 | 分值 | 患者比例(%) | 5年总生存率(%) | 10年总生存率(%) |
| 低危 | 0或1 | 36 | 90.6 | 70.7 |
| 中危 | 2 | 37 | 77.6 | 50.9 |
| 高危 | 3~5 | 27 | 52.5 | 35.5 |
滤泡性淋巴瘤国际预后指数2(Folicullar lymphoma IPI 2,FLIPI2)
| 项目 | 0分 | 1分 |
| 年龄(岁) | <60 | ≥60 |
| 血红蛋白水平 | ≥120g/L | <120g/L |
| 淋巴结最长径 | ≤6cm | >6cm |
| β2微球蛋白 | 正常 | 升高 |
| 骨髓 | 未受侵 | 受侵 |
滤泡性淋巴瘤国际预后指数2的风险分组与生存率
| 风险组 | 分值 | 5年总生存率(%) | 5年无进展生存(%) |
| 低危 | 0或1 | 98% | 79% |
| 中危 | 2 | 88% | 51% |
| 高危 | 3~5 | 77% | 20% |
附件3.4
套细胞淋巴瘤预后评分
简化的套细胞淋巴瘤国际预后指数(Mantle cell lymphoma IPI,MIPI)
| 评分 | 年龄 | ECOG | LDH x正常上限 | 白细胞(x109/L) |
| 0 | < 50 | 0~1 | < 0.67 | < 6.7 |
| 1 | 50~59 | -- | 0.67~0.99 | 6.7~10 |
| 2 | 60~69 | 2~4 | 1.0~1.49 | 10 ~ 15 |
| 3 | ≥ 70 | -- | ≥1.5 | ≥ 15 |
ECOG(Eastern Cooperative Oncology Group,美国东部肿瘤协作组);LDH(lactate dehydrogenase,乳酸脱氢酶)
简化的套细胞淋巴瘤国际预后指数与生存
| 风险组 | 分值 | 中位生存期(月) |
| 低危 | 0~3 | 未达到 |
| 中危 | 4~5 | 51 |
| 高危 | 6~11 | 29 |
联合Ki-67的套细胞国际预后指数(MIPIc)
| MIPIc | MIPI | Ki-67 | 患者比例(%)GLSG(n=246) | 患者比例(%)EMCLN(n=508) | 5年OS(%)EMCLN | 中位OS(年)GLSG |
| 低危 | 低危 | <30% | 32 | 44 | 85 | 9.4 |
| 低中危 | 低危 | ≥30% | 5 | 9 | 72 | 4.9 |
| 中危 | <30% | 25 | 29 | |||
| 高中危 | 中危 | ≥30% | 6 | 10 | 43 | 3.2 |
| 高危 | <30% | 10 | 13 | |||
| 高危 | 高危 | ≥30% | 5 | 11 | 17 | 1.8 |
GLSG(German Low-Grade Lymphoma Study Group,德国低度恶性淋巴瘤研究组); EMCLN(European Mantle Cell Lymphoma Network,欧洲套细胞淋巴瘤协作网)
3.5 外周T细胞淋巴瘤(非特指型)预后评分(PIT)
| 项目 | 0分 | 1分 |
| 年龄(岁) | ≤60 | >60 |
| 骨髓受侵 | 无 | 有 |
| ECOG评分 | 0或1 | 2~4 |
| LDH | 正常 | 升高 |
ECOG(Eastern Cooperative Oncology Group,美国东部肿瘤协作组);LDH(lactate dehydrogenase,乳酸脱氢酶)
| 分值 | 5年总生存率(%) | 10年总生存率(%) |
| 0 | 62.3 | 54.9 |
| 1 | 52.9 | 38.8 |
| 2 | 32.9 | 18.0 |
| 3~4 | 18.3 | 12.6 |
附件4 恶性淋巴瘤疗效判定标准
附件4.1 Deauville五分量表
| 1 | 无FDG摄取 |
| 2 | 有摄取但SUV低于纵隔血池 |
| 3 | SUV介于纵隔血池和肝脏之间 |
| 4 | SUV稍高于肝脏 |
| 5 | SUV明显高于肝脏或为出现新病灶 |
| X | 新出现的有摄取的区域,与淋巴瘤没有关系 |
| 注:SUV(Standarized uptake value)标准摄取值 | |
附件4.2
Cheson疗效判定标准(CT/MRI)
| 疗效 | 体格检查 | 淋巴结 | 融合淋巴结 | 骨髓 |
| CR | 正常 | 正常 | 正常 | 正常 |
| CRu | 正常 | 正常 | 正常 | 未确定 |
| 正常 | 正常 | 缩小>75% | 正常或未确定 | |
| PR | 正常 | 正常 | 正常 | 受侵 |
| 正常 | 缩小≥50% | 缩小≥50% | 无关 | |
| 肝/脾缩小 | 缩小≥50% | 缩小≥50% | 无关 | |
| 复发/进展 | 肝/脾增大,新病灶 | 新病灶或增大 | 新病灶或增大 | 重新出现受侵 |
CR(complete remission,完全缓解);CRu(uncomfirmed complete remission,CRu,完全缓解未确定);PR(partial response,部分缓解)
附件5
我国未批准上市,美国FDA批准上市用于治疗淋巴瘤的主要新药和适应证
| 药品名称 | 作用机制 | FDA批准适应证 | 批准上市时间 |
| 阿仑单抗,Alemtuzumab | 人源化CD52单抗 | 烷化剂和氟达拉滨耐药的进展期CLL | 2001年5月 |
| 贝利司他,Belinostat | 组蛋白去乙酰化酶抑制剂 | 复发、难治的外周T细胞淋巴瘤 | 2014年7月 |
| 苯达莫司汀,Bendamustine | 双功能基烷化剂 | 1.CLL 2.惰性B细胞淋巴瘤 | 2008年3月 |
| Brentuximab vedotin | CD30单抗偶联细胞毒素MMAE(monomethyl-auristatin-E) | 1.自体造血干细胞移植后失败或不适合自体造血干细胞移植,至少二线治疗失败的cHL 2.自体造血干细胞移植后高复发或进展风险患者的巩固治疗 3.经一线多药联合方案化疗后失败的系统性间变大细胞淋巴瘤(ALCL) | 2011年10月 |
| 4.复发难治原发性皮肤间变性大细胞淋巴瘤(pcALCL)和表达CD30的蕈样肉芽肿(MF) | 2017年11月10日 | ||
| 5.与化疗联合治疗先前治疗过的的III期或IV期cHL | 2018年3月20日 | ||
| Idelalisib | 选择性PI3Kδ(磷脂酰肌醇3激酶)抑制剂 | 1.联合利妥昔单抗治疗复发的CLL 2.至少二线以上化疗失败的FL和CLL | 2014年7月 |
| 伊布替尼,Ibrutinib | BTK抑制剂 | 1.至少一线治疗失败的MCL 2.一线治疗失败的CLL 3.17P缺失的CLL 4.华氏巨球蛋白血症 | 2013年11月 |
| 来那度胺,Lenalidomide | 免疫调节剂 | 二线治疗失败的MCL | 2013年5月 |
| Obinutuzumab | 人源化和糖基化CD20单抗 | 联合苯丁酸氮芥治疗初治CLL | 2013年11月 |
| 奥法木单抗,Ofatumumab | 全人源化CD20单抗 | 氟达拉滨治疗无效的顽固性CLL | 2014年4月 |
| 普拉曲沙,Pralatrexate | 叶酸代谢抑制剂 | 复发或难治性外周T细胞淋巴瘤(PTCL) | 2009年9月 |
| 罗米地辛,Romidepsin | 组蛋白去乙酰化酶抑制剂 | 一线治疗失败的皮肤T细胞淋巴瘤 | 2009年11月 |
| 伏立诺他Vorinostat | 组蛋白去乙酰化酶抑制剂 | 二线治疗失败的皮肤T细胞淋巴瘤 | 2006年10月 |
| Copanlisib | 选择性PI3Kδ(磷脂酰肌醇3激酶)抑制剂 | 至少二线以上化疗失败的FL | 2017年9月15日 |
| acalabrutinib | BTK抑制剂 | 至少一线治疗失败的MCL | 2017年11月1日 |
| Yescarta | anti-CD19 CAR-T | 复发/难治性大B细胞淋巴瘤 | 2017年10月18日 |
| nivolumab | PD-1单抗 | HDC/AHSCT后进展或不能接受移植且先前接受过三种化疗进展的cHL | 2016年5月17日 |
| pembrolizumab | PD-1单抗 | 难治性以及既往接受过3种或3种以上方案治疗后病情复发的cHL | 2017年3月14日 |
| obinutuzumab | 人源化和糖基化CD20单抗 | 与化疗药物联合治疗先前未经治疗的晚期FL | 2017年11月21日 |
FDA(Food and Drug Administration,食品药品管理局);CLL(chronic lymphocytic leukemia,慢性淋巴细胞白血病);MCL(mantle cell lymphoma,套细胞淋巴瘤);FL(Follicular lymphoma,滤泡淋巴瘤);cHL(classical Hodgkin lymphoma,经典霍奇金淋巴瘤)
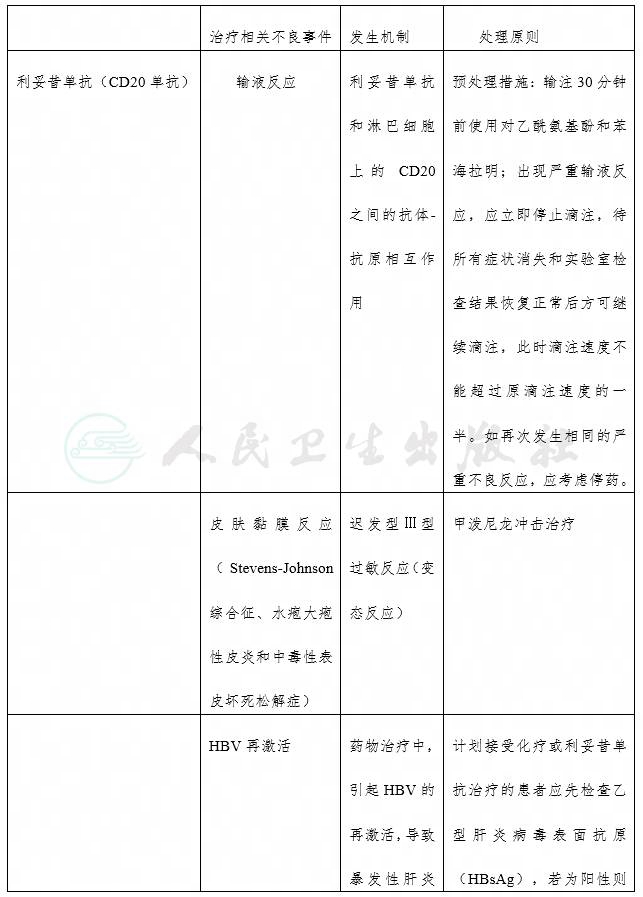
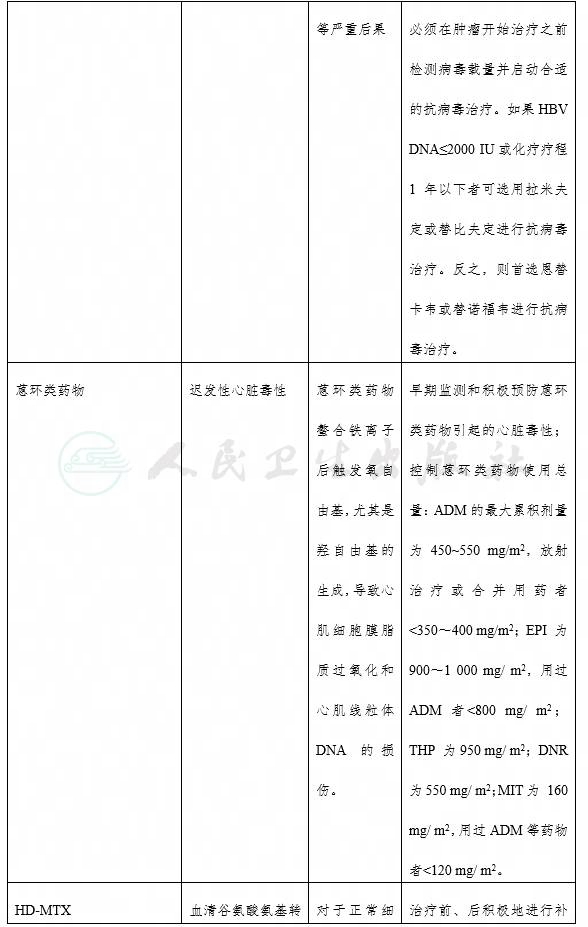
附件6
淋巴瘤治疗特殊药物相关不良事件汇总